Electroquímica Ambiental, Estudio de Electrodiálisis de Aguas Residuales
Introducción
La idea de que la humanidad está trabajando para
su autodestrucción como lo propone de forma risible Rubens
Ramalho gracias a un proceso sistemático de
contaminación se ha venido estructurando a nivel mundial
aproximadamente desde mediados de la década de los 70.
Desde entonces el sentido de protección ambiental ha
evolucionado de forma notable y se puede asegurar que hoy
más que nunca prácticamente todos los procesos
industriales tienen dos objetivos básicos; ser eficientes
y sobre todo tener un impacto ambiental mínimo. Dentro del
contexto nacional, solo en la última década, la
legislación de protección animal, vegetal y
ambiental a determinado ciertos parámetros para mantener
mejor controlados los residuos de lechos industriales,
fábricas y microempresas que puedan generar algún
daño irreparable a la naturaleza.
En Quito, la primera ordenanza municipal de control que
regulaba en alguna medida la emisión de CO(g) a la
atmosfera, así como las descargas industriales liquidas
(Ordenanza Metropolitana 012) data del 9 de Noviembre de 1998,
(es decir poco más de 15 años).
En el año 2000 en una nueva ordenanza (Ordenanza
metropolitana 31) se establecía por primera vez los
valores máximos permisibles de los indicadores de
contaminación y parámetros para descargas liquidas
industriales, ambas fueron derogadas en el 2005 por la ordenanza
146 cuyo marco legal era mucho más amplio, estricto y
mantenía parámetros a estándares
internacionales, aun así las penalizaciones no eran
económicamente perjudiciales para las grandes empresas
pero en cambio se dispuso por primera vez controles de parte de
una entidad de seguimiento a cada una de las grandes y medianas
industrias que generaran desechos, cada una de estas entidades
reportaban los resultados directamente al municipio que cobraba
multas por las faltas ambientales que se cometiesen. La
última derogación se dio en el 2007 con la
ordenanza 213 que elevo las tazas de penalización, y
dentro del marco legal hasta se contempla el cierre de la
fábrica si en un lapso de tiempo no logra minimizar el
impacto ambiental en sus procesos industriales.
La legislación ambiental nacional está muy
retrasada con respecto a la legislación de países
como Estados Unidos, en donde a partir del 1 de Julio de 1983 los
únicos residuos permitidos en un proceso industrial
serán Hidrogeno, Oxigeno, Dióxido de carbono, agua
y algo (no demasiado de calor residual) aproximadamente 15
años de retraso en cuanto a parámetros para
descargas industriales.
Varios estudios indican que es menos costoso para las
distintas industrias reducir los indicadores de
contaminación durante el proceso que en la descarga final
invirtiendo grandes cantidades de dinero en plantas de
tratamiento de aguas de costos elevados, por ello una de las
soluciones a futuro a la que debe plantearse y lograr la
industria nacional es ser eficiente en el gasto monetario y
reducir los parámetros contaminantes durante el proceso de
producción para asi no realizar grandes inversiones, se
puede observar el siguiente diagrama.

Figura 1. Efecto de la
Reducción de carga contaminante en los costes de
inversión de una planta de tratamiento
Fuente: (Chemical Engineering-1973
Mayo 14, McGraw-Hill)
La corrección de la contaminación no es un
problema técnico de gran dificultad, en si el conocimiento
técnico básico requerido para resolver el problema
de la contaminación esta ya a disposición de la
sociedad y básicamente se necesita visión
innovadora y un gran capital inicial para ajustar y reducir el
nivel de contaminantes de las descargas industriales.
Grados de Tratamiento de Aguas Residuales y
Parámetros de calidad de aguas de
Descarga
Muchas empresas a nivel mundial buscan reducir los
niveles de contaminación ambiental no necesariamente por
una conciencia ecológica sino por evitar las elevadas
multas tipificadas en la legislación de cada ciudad o
país, es por ello que se han desarrollado tres niveles de
tratamientos de agua residuales donde se podrá notar que
el nivel de inversión y por consiguiente técnico
aumenta de forma ascendente por cada nivel. El nivel uno
(denominado tratamiento primario) se emplea para la
eliminación de sólidos en suspensión,
coloides y materiales flotantes, en este nivel se utiliza la
sedimentación, filtración, separación de
aceites, neutralización, etc (que como puede analizarse
son tratamiento básicamente físicos de un costo no
muy elevado y sobre todo del que no se necesita una
infraestructura compleja). En el nivel dos se encuentran los
tratamientos biológicos convencionales como
aireación con oxígeno puro (proceso de
oxidación total), filtros biológicos (bacterias que
descomponen la materia orgánica), lodos activos (cultivo
bacteriano en forma de floculas en medio de aguas residuales con
aireación y agitación, dentro del nivel dos el
más común a nivel industrial por sus resultados).
Finalmente el nivel tres tiene como objetivo eliminar los
contaminantes que no se eliminan con los tratamientos
biológicos convencionales, aquí podemos encontrar
el microtamizado, la osmosis inversa, electrodiálisis,
cloración e intercambio iónico.( Para más
información ver Pg 9, RAMALHO, Tratamiento de Aguas
Residuales).
Muchas de las normas de calidad dentro de los
parámetros legales dependerán del uso del agua,
algunas de estas incluyen pH, color, turbidez, dureza (mg/L),
solidos disueltos totales (SDT, mg/L), sólidos en
suspensión (SS, mg/L), concentración de
oxígeno disuelto (OD, mg/L), olor temperatura,
etc.
Tipos de Contaminantes de Agua y
suministros
Los suministros naturales del agua se clasifican en tres
diferentes categorías; La primera son las aguas
superficiales que comprenden ríos, lagos, océanos y
embalses. De esta lista (para las aguas superficiales) se puede
suponer que en los ríos u océanos sometidos a
contaminación, la calidad de agua es variable a lo largo
del curso del cauce, en cambio en lagos o en presas, la calidad
del agua es casi constante. El segundo tipo de suministro natural
son las aguas subterráneas, que presentan menor turbidez
que las aguas superficiales y el tercer tipo son las aguas
meteorológicas (agua lluvia, nieve, granizo, etc) que
presentan las mayores propiedades de pureza
físico-química que el resto.
Los tipos de contaminantes del agua también son
tres; El primer tipo son los contaminantes químicos que
comprenden productos químicos orgánicos e
inorgánicos (estos últimos podrían poseer un
efecto toxico), además no presentan una gran demanda por
oxígeno. Los contaminantes de origen orgánico
(gracias al oxigeno del ambiente) puede degradarse, dando como
resultado una variación de la actividad biológica
del medio.
Existen casos donde los compuestos inorgánicos
(como los sulfitos y nitritos reaccionan con el oxígeno
para convertirse en nitratos y sulfatos respectivamente) son
iones de metales pesados muy tóxicos para seres humanos,
principalmente se presentan en las aguas residuales de las
industrias de pinturas, textiles y plásticos. El mercurio,
arsénico, cobre, zinc, níquel, cromo, plomo, cadmio
son ejemplos de estos metales pesados muy tóxicos
inclusive en concentraciones mínimas.

Los contaminantes físicos incluyen
contaminación térmica (aguas procedentes de plantas
industriales), turbidez (aguas que contienen sólidos en
suspensión), espumas (detergentes), radiactividad. Los
contaminantes biológicos pueden transmitir enfermedades
como cólera, tifoidea, o indigestión.
Definiciones Importantes
1. Demanda Teórica de
Oxigeno
La demanda teórica de oxigeno referida como
[DTeO]es la cantidad estequiometrica de oxigeno requerida para
oxidar por completo un compuesto químico (orgánico
e inorgánico) esta expresada en [mg/L]
2. Demanda Química de Oxigeno
(DQO)
La demanda Química de Oxigeno referida como [DQO]
es el volumen de oxigeno requerido para oxidar la fracción
orgánica de una muestra susceptible de oxidación en
medio acido con el ion permanganato o dicromato como agentes
oxidantes. El DQO no es exactamente igual al [DTeO], en promedio
para que se considere que el valor es correcto este debe ser
alrededor del 80-85% del [DTeO]. (Para averiguar acerca de los
métodos experimentales de determinación del DQO con
distintos agente oxidantes ver en SHUN DAR LIN, Water and
Wastewarer Calculations Manual, Second Edition,pg 52).
3. Demanda Bioquímica de Oxigeno
(DBO)
La demanda Bioquímica de oxigeno referida como
(DBO) es la medida de la cantidad de oxigeno requerido para
oxidar la materia orgánica biodegradable presente en la
muestra de agua (oxidación bioquímica anaerobia).
Básicamente el DBO es el resultado de la
biodegradación de materiales orgánicos
carbónicos (utilizados como fuente de alimento de
organismos aeróbicos), nitrógeno oxidable
(derivados de la presencia de nitritos, amoniaco y en general
compuestos orgánicos nitrogenados) y de compuestos
químicos reductores (como ion ferroso, sulfitos, sulfuros,
que se oxidan con oxígeno)
4. Demanda Total de Oxigeno
(DTO)
La determinación de la demanda total de oxigeno
prevé la utilización de un sistema
químico-instrumental mucho más complejo (Ver
RAMALHO, Tratamiento de Aguas Residuales, ed Reverte,
México D.F, tercera edición, pg 45),
básicamente se mide el total del oxígeno consumido
de las siguientes reacciones:

De toda esta sección se puede mostrar el
siguiente diagrama donde se comparan las cantidades de DTO,DQO y
DBO para una muestra de agua con relación al tiempo de
estudio de la misma.

Figura 2. Analisis Semanales de
Aguas residuales originales
Fuente: American Chemical
Society-18 Octubre-1992
Bibliografía:
NEMEROW L. NELSON, Tratamiento de
vertidos Industriales y peligrosos, Madrid, 1998 tercera
edición. (Link google books:
http://books.google.com.ec/books?id=KDmjTWMEuaoC&printsec=frontcover#v=onepage&q&f=false)Ordenanzas Municipales Quito (Link:
http://www7.quito.gob.ec/mdmq_ordenanzas/Ordenanzas/ORDENANZAS/ORDENANZAS%20MUNICIPALES%202013/)RAMALHO, Tratamiento de Aguas
Residuales, México D.F, Ed Reverte, Tercera
edición, 1993)SHUN DAR LIN, Water and Wastewarer
Calculations Manual, Second Edition,1998.
Procesos
electroquímicos para tratamiento de aguas
residuales
Prácticamente la mayoría de los compuestos
contaminantes y tóxicos pueden sufrir reacciones de
reducción u oxidación, como ejemplo se propone que
el Cromo VI (en forma de iones cromato) es un compuesto sumamente
toxico (puede alterar el ADN y producir alteraciones
genéticas), mientras que el Cromo III casi no lo es, es
decir con una simple transferencia de electrones (en este caso
una reducción) el nivel de toxicidad disminuye de forma
abismal. De esta misma forma se puede proceder con la
reducción u oxidación de distintos tipos de
compuestos tóxicos para el ser humano o
ambiente.
La mayoría de estas reacciones de
óxido-reducción se pueden realizar en electrodos o
superficies electrificadas, además los procesos
electroquímicos ofrecen una gran facilidad y factibilidad
para el estudio de contaminantes de aguas residuales así
como rapidez, confiabilidad y hasta un coste económico
reducido en comparación con otro tipo de métodos de
laboratorio.
2.1. Electrodiálisis
En un inicio la electrodiálisis (tratamiento
terciario para aguas residuales) fue diseñada para la
desalación del agua de mar (principalmente en
países con escasas reservas de agua como Kuwait, Arabia
Saudita e Israel) pero actualmente no solo es utilizado para ese
fin, pues nuevas investigaciones concluyen que sirve
también para la eliminación de compuestos
inorgánicos como fosforo y nitrógeno de las aguas
residuales. El componente principal que conforma la celda de
electrodiálisis son las membranas de resina para el
intercambio iónico, que justamente son permeables para el
paso de aniones o cationes, existen dos tipos de
membrana;
El primer tipo es la membrana catódica, que posee
una carga negativa que permite a los iones positivos (cationes)
pasar a través de dicha membrana repeliendo al paso de
aniones (iones negativos). El segundo tipo son las membranas
anionicas que están cargadas positivamente y de forma
análoga a la membrana anteriormente mencionada solo
permite el paso de aniones (iones negativos) repeliendo al paso
de cationes (iones positivos)

Figura 3. Diagrama Básico
de una celda de electrodiálisis
Fuente: ALONSO VANTE
NICOLÁS, Electroquímica y Electrocatálisis
Tomo II, primera edición 2003, México D.F, pg
637
El proceso de la electrodiálisis se lo debe
efectuar con la aplicación de una tensión
eléctrica a lo largo del sistema de la figura 3. Para
armar el sistema el cátodo y el ánodo se colocan en
los extremos de la celda con el objetivo que de que la membrana
más próxima al cátodo sea permeable a los
cationes y la más próxima al ánodo sea
permeable a los aniones. Para volver más eficiente al
sistema la materia coloidal y las partículas en
suspensión deben separarse antes del proceso (es por ello
que es un tratamiento terciario para aguas residuales) pues caso
contrario la resistencia eléctrica generada por estas
partículas será mayor.
2.2. Detección de Sustancias
Contaminantes
Los electrodos sensores son dispositivos de
medición usados para la detección de sustancias
contaminantes, su funcionamiento en teoría corresponde a
las reacciones de óxido- reducción en medio acuoso,
a más de ello se puede realizar una detección en
compuestos sólidos, gaseosos y líquidos inmiscibles
en agua, este método permite determinar (gracias a la
ecuación de Nerst) la tensión formada en cada una
de las disociaciones iónicas presentes. Los electrodos
más desarrollados son los de membrana que se utilizan para
determinar la concentración de iones o para realizar
mediciones de pH
Otro tipo de sensores son las celdas de conductividad y
los sensores fotoelectroquimicos, ambas basan su funcionamiento
en las propiedades conductoras y fotoconductoras de un compuesto
por la presencia de sustancias contaminantes.
Mecanismos Electroquímicos para la
oxidación o reducción de sustancias y
Diseño de Reactores para tratamiento de desechos
contaminantes
Para determinar el proceso electroquímico el cual
aplicar para oxidar o reducir a un compuesto contaminante de las
aguas residuales, se debe conocer de antemano las condiciones de
pH, conductividad eléctrica y sobre todo el material de
los electrodos adecuados así como tensión formada
en la celda. Muchos de los principales procesos para degradar
compuestos contaminantes son aquellos enfocados al tratamiento de
soluciones de iones metálicos como el plomo II, Cobre II,
mercurio II, plata I y cromo (VI).
Muchas veces en las reacciones de oxidación o
reducción (sobre todo de los contaminantes por compuestos
orgánicos donde existe un gran número de electrones
transferidos) se pueden formar diversas reacciones paralelas y
por tanto la formación de especies químicas
intermedias, por ejemplo las reacciones de polimerización,
para este tipo de reacciones se debe tomar muy en cuenta el
material del electrodo, dado que se busca priorizar la
reacción principal. Los materiales más utilizados
como cátodos son los aceros inoxidables y carbón
vítreo (desarrollado en la década de los 60 en
Reino Unido, en un inicio se utilizaba celulosa como material
para obtener el polímero). Para los ánodos son
utilizados los óxidos metálicos de: Ru, Ti, Ir, Pb,
Sn o Pt que catalizan reacciones redox y además por
presentan una buena resistencia a la corrosión.
Para realizar el diseño de un reactor
electroquímico se debe lograr el objetivo de tener un
diseño eficiente se deben tomar en cuenta factores que
incidan en el funcionamiento del mismo tales como materiales del
electrodo, solución electrolítica, geometría
de la celda, velocidades de flujo, temperatura y gasto de
energía eléctrica. Los diseños de reactores
más exitosos para el tratamiento de aguas están los
que utilizan electrodos tridimensionales y configuraciones de los
mismos en paralelo.
Procesos Directos e Indirectos
Existen celdas electroquímicas donde es posible
transferir electrones directamente desde un electrodo hacia una
especie electroactiva (sustancia con carácter oxidante y
reductor que es capaz de transportar carga sin sufrir
modificaciones atómicas) y viceversa, a este proceso se le
denomina directo. En cambio existen celdas electroquímicas
donde no es posible transferir electrones directamente debido a
que los compuestos a separar no son especies electroactivas, en
estos casos se pueden utilizar compuestos que se generan como
parte de las reacciones segundarias de una electrolisis que
actúan como mediadores (denominados acarreadores) que
ayudan a la transferencia de electrones desde y hacia los
compuestos a oxidar o reducir, este tipo de proceso se denomina
proceso indirecto.

Figura 4. Clasificación de
los Reactores Electroquímicos, según la
geometría y el movimiento de los electrodos
Fuente: ALONSO VANTE
NICOLÁS, Electroquímica y Electrocatálisis
Tomo II, primera edición 2003, México D.F, pg
165
Procesos Directos
Oxidaciones Directas
Compuestos Inorgánicos
Se debe recordar de antemano que en un reactor
electroquímico las reacciones de reducción y
oxidación se dan en el cátodo y ánodo
respectivamente sin importar el tipo de pila o reactor que este
sea, es por ello que para la oxidación el electrodo
más importante para el proceso será el
ánodo, así que su proceso de selección (es
decir seleccionar el material, su composición,
estabilidad, pH y sobre todo su conductividad y reactividad con
los compuestos a oxidar.

El material más común con el que se
trabaja para el ánodo es el óxido de plomo pues
reduce grandemente el nivel de oxidación del agua, y al
contrario ayuda a la producción de oxigeno
(reducción del agua), tiene además la ventaja de
ser un compuesto con mucha estabilidad, barato y es utilizado
también para los compuestos orgánicos, sin embargo
es toxico pues puede alcanzar a emitir iones de plomo al
ambiente. Se utiliza también electrodos recubiertos con
óxidos de metales nobles, diferentes tipos de electrodos
de cambón (grafito, carbón vítreo),
níquel (para valores altos de pH), titanio, acero
inoxidable, ebonex (oxido de titanio conductor),etc. No es
posible hablar de un ánodo universal, por lo que en cada
caso debe evaluarse el desempeño de los materiales
candidatos. Por ejemplo, por encima de ciertos potenciales el
oxígeno proveniente de la oxidación del agua entra
en los planos basales del grafito y produce ruptura. Asimismo, el
acero inoxidable empieza a oxidarse a ciertas condiciones de
potencial y pH por lo que su utilidad bajo estas condiciones es
nula.
La sustancia inorgánica toxica que se oxida por
las celdas electroquímicas es el ion cianuro. El
método tradicional de oxidación es
agregándole una concentración conocida de ion
hipoclorito, pero se puede diseñar una celda con
electrodos de óxido de plomo para llegar al mismo fin, el
ion oxidado es el ion cianato el cual es casi inicuo para la
salud humana.
Compuestos Orgánicos
Fenoles
Los compuestos fenólicos poseen un grado
mínimo de toxicidad, y en soluciones acuosas tiene un olor
desagradable y se oxidan hasta la formación de
dióxido de carbono. Al ser un compuesto aromático
con grupos hidroxilo pueden polimerizarse sobre el electrodo y
dificultar la transferencia de electrones, siendo este
último fenómeno en la producción de
anticorrosivos. En la siguiente grafica se expone la
disminución de la concentración de fenol en aguas
residuales con este tipo de componentes a presiones
distintas.
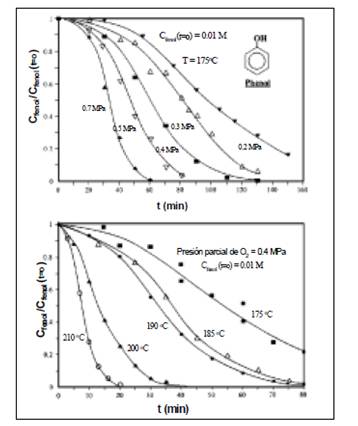
Figura 5. Diagrama de la
concentración de Fenol a distintas presiones (grafico
superior) y distintas temperaturas (grafico inferior) vs el
tiempo (min)
Fuente: NEMEROW L. NELSON,
Tratamiento de vertidos Industriales y peligrosos, Madrid, 1998
tercera edición. (Link google books:
http://books.google.com.ec/books?id=KDmjTWMEuaoC&printsec=frontcover#v=onepage&q&f=false)
Aminas
Aromáticas
Las aminas aromáticas los hacen peligrosas para
la salud humana pues pueden formar complejos con la hemoglobina
de la sangre y así intoxicar a todo el cuerpo, son tan
reactivas como el oxígeno, se utiliza prácticamente
los mismos electrodos que los compuestos fenólicos para su
oxidación.
Compuestos
Halogenados
Los compuestos halogenados son conocidos por su
toxicidad, a mayor número de halógenos en la
molécula más toxica esta última será.
La oxidación de estos halógenos se puede realizar
mediante una reacción nucleofilica con producción
de cloro gaseoso. (Es un procedimiento un tanto toxico y
contaminante)
Reducciones Directas

Compuestos Orgánicos
Muchos hidrocarburos clorados han sido clasificados como
tóxicos y hasta cancerígenos, la reacción
general para la reducción de compuestos orgánicos
es la siguiente.

La gran ventaja de esta reacción es que se puede
utilizar cualquier ion para la remoción del haluro,
produciendo siempre un compuesto tipo R-H (que depende del ion
utilizado) y este nuevo compuesto puede ser biodegradado
posteriormente evitando la contaminación
ambiental.
Compuestos Inorgánicos
1) Cromatos
Los iones cromo (VI) son muy tóxicos para los
seres humanos, para lograr su reducción se utilizan
electrodos de grafito y así se los reduce a cromo
(III).
2) Iones Oxiclorados
Durante la desinfección de aguas por medio de
cloro, se producen iones clorito y clorato, hipoclorito o
dióxido de cloro, estos iones se pueden reducir
directamente hasta el ion cloruro que no presenta problemas al
medio ambiente.
3) Iones Oxinitrados
En los desechos agroindustriales los nitratos
están presentes en muchas corrientes procedentes de
desechos de agricultura y en pozos de agua. Estas aguas
contaminadas poseen las bacterias como la E. Coli y hasta se han
documentado casos de síndrome azul en niños menores
de edad gracias a la bacteria antes mencionada, que es capaz de
reducir los nitratos a nitritos en el intestino de los bebes los
cuales pueden formar complejos con la hemoglobina y ocupar el
lugar del oxígeno en la sangre.
En los tratamientos a sustancias nucleares se produce la
reducción directa de los nitratos a nitritos y
subsecuentemente reducción produciendo nitrógeno,
óxido nitroso o amoniaco como se expresa en las siguientes
reacciones.

4) Iones Metálicos
Las aguas residuales con alta concentración de
iones metálicos tienen origen en las industrias de
recubrimientos metálicos y refinación de metales,
metales y metaloides como Aluminio, Arsénico, Cadmio,
Cobre, Cromo, Mercurio, Níquel, Plata y Plomo. Se ha
demostrado que mientras más baja sea la
concentración de estos metales pesados en solución
(concentraciones por debajo de los 10ppm) más complejo
será el desarrollo el proceso que ayude a disminuir su
concentración en medio acuosa.
Una de las grandes soluciones que se han establecido es
la selección (para el proceso electroquímico) es la
selección de electrodos porosos (de acero inoxidable y
carbón vítreo), y el diseño del reactor con
sistemas de flujo. Por ejemplo para remover el ion Pb (II),
resulta más eficiente la reducción con electrodos
de acero inoxidable. Uno de los iones de metales pesados
más tóxicos y de más difícil
reducción a nivel industrial es el Cr (VI), siendo este
ion un metal muy reactivo, tiene la capacidad de oxidar el agua,
alterando con esto su calidad, prácticamente todos los
trabajos para la reducción de este ion van encaminados a
reducir de Cr (VI) a Cr (III). Uno de los procesos más
utilizados se da por medio del Fe( II) en solución acuosa,
otro mecanismo de reducción del Cr (VI) se da cuando esta
reducción se da sobre solidos recubiertos de
polímeros específicamente con el polipirrol que
posee propiedades reductoras y es oxidado sobre superficies de
carbón vítreo o metales nobles como oro o platino.
El polipirrol entra en contacto con una solución de
cromatos, además transfiere de forma espontánea
electrones al cromato, reduciéndolo y así
disminuyendo su toxicidad de forma radical.
Procesos Indirectos
1. Oxidaciones Indirectas
En la oxidación directa de compuestos
orgánicos, se debe tomar en cuenta la gran cantidad de
electrones que se involucran y la gran cantidad de compuestos
intermediarios que se forman, y además las reacciones de
polimerización que pueden cambiar las propiedades de la
superficie del electrodo. Los procesos indirectos en cambio
consisten en formar un agente oxidante y otro reductor en el
ánodo y el cátodo, que posteriormente en
solución se encargara de oxidar y reducir el DQO y el DBO
hasta niveles permisibles.

El resto de agentes oxidantes que oxidan a compuestos
orgánicos son iones metálicos en estados de
oxidación más altos o iguales que el número
de letras de sus iniciales, por ejemplo el Ag (II) que es uno de
los mejores agentes oxidantes para compuestos orgánicos de
fosfatos, orgánicos de azufre y de cloro, tanto
alifáticos como aromáticos.
En soluciones donde se producen iones cloruro, no es
posible utilizar el ion Ag (II) pues el precipitado formado
será AgCl, para este tipo de casos se utiliza al Co (III)
como oxidante. En cambio el Fe (III) es también un agente
oxidante que se utiliza principalmente para procesos de
degradación de grasas, materiales derivados de la
celulosa, urea, desechos de empaque de carne, agua de drenaje y
combustibles fósiles.
El ion Ce (IV) es conocido como un excelente oxidante
para destruir organismos contaminantes y residuos de combustible
convirtiéndolos en CO2.
La formación de iones OH- en el cátodo del
reactor electroquímico puede facilitar la remoción
de las partículas culpables de la dureza del agua como se
explica en las siguientes reacciones:

A más de los compuestos contaminantes presentes
en las descargas de aguas industriales, se pueden encontrar
emulsiones formadas de agua y líquidos inmiscibles
dispersos (muy comunes de las gasolinas y de los sitios de
extracción petrolera). Para combatir este tipo de
contaminación se utiliza un campo eléctrico que
desestabiliza la polaridad de la emulsión. Además
se puede combinar agentes coagulantes (o floculantes, como
Hidróxidos de Al, Fe (II), y Fe (III)) con la
producción de un gas (comúnmente Hidrogeno), lo que
da como resultado una floculación –
coagulación que adsorbe los contaminantes presentes. Los
lodos resultantes poseen baja densidad lo que posibilita su
separación con mucha facilidad.
Reducciones Indirectas

Procesos Híbridos para el tratamiento de
Desechos acuosos
Existen alternativas hibridas para realizar
degradaciones parciales, por ejemplo transformar la materia no
biodegradable en biodegradable, también se puede combinar
uno o dos procesos electroquímicos con u proceso
catalítico, este último es utilizado para tratar el
agua de desecho en el hogar.

Bibliografía
NEMEROW L. NELSON, Tratamiento de vertidos
Industriales y peligrosos, Madrid, 1998 tercera
edición.ALONSO VANTE NICOLÁS, Electroquímica y
Electrocatálisis Tomo II, primera edición 2003,
México D.F,SHUN DAR LIN, Water and Wastewarer
Calculations Manual, Second Edition,1998.RAMALHO, Tratamiento de Aguas
Residuales, México D.F, Ed Reverte, Tercera
edición, 1993)B.B.DAMASKIN, O.A.PETRI, Fundamentos de la
Electroquimica Teorica Tomo I y II, Ed Mir, segunda
edición, Moscu, 1981.ZOSKI C,Handbook of Electrochemistry, New Mexico
State University, first edition, 2007.
Autor:
Jhonattan Manosalvas
Paralelo 1
UNIVERSIDAD CENTRAL DEL ECUADOR
FACULTAD DE INGENIERIA QUIMICA
INGENIERIA QUIMICA
Electroquímica
Monografía Final,
18 de Diciembre 2013
Quito-Ecuador
