- Definición
- Tipos de
osteomielitis - Métodos
diagnósticos - Algoritmo
diagnóstico - Diagnóstico
diferencial - Tratamiento
- Bibliografía
La osteomielitis es una infección de la cortical
y medular del hueso, generalmente de origen bacteriano, aunque
puede estar producida por cualquier microorganismo. La clasificación se puede
hacer según un gran número de criterios
(etiología, patogenia, localización, evolución, etc.), pero las más
utilizadas son la patogénica de Waldvogel, que considera
tres clases: hematógena, por contigüidad y asociada a
insuficiencia vascular; y la de Cierny y Mader que establece doce
grupos
combinando la localización anatómica y la
situación del huésped, y cuyo propósito es
estandarizar el tratamiento.
- La causa más frecuente es la bacteriana,
aunque también pueden ser de origen vírico y
producido por hongos
(generalmente en el contexto de una infección
sistémica). Varía según la
edad. - Staphyloccocus aureus es el principal patógeno
en todas las edades, ocasiona el 90% de las osteomielitis
agudas. - El segundo en orden de frecuencia es Streptoccocus
betahemolítico del grupo A
(SBHGA) (menos de un 10% de casos). Haemophilus influenzae
puede ser responsable de OA en niños
no vacunados. - En neonatos juegan un papel importante Streptococcus
del grupo B y los bacilos gramnegativos (E. Coli). - En zonas de punción a nivel plantar el
principal patógeno implicado es Pseudomonas aeuruginosa
y también otros bacilos gramnegativos. Es frecuente en
mayores de 6 años. - En niños con anemia de
células
falciformes deberá investigarse la presencia de
Salmonella. - Deben sospecharse otros microorganismos según
la patología de base y la puerta de entrada.
Además de los neonatos y de los pacientes con
drepanocitosis, existen otros grupos de riesgo:
hemodializados, con fracturas cerradas o con osteomielitis
multifocal crónica recurrente.
PATOGENIA
Existen tres tipos de osteomielitis:
- Osteomielitis aguda hematógena, secundaria a
bacteriemia: Forma más frecuente. - Osteomielitis no hematógena, por
inoculación directa: Ocurre tras un traumatismo o
cirugía o por diseminación a partir de un foco
contiguo, generalmente celulitis. - Osteomielitis crónica: Se produce de forma
secundaria a un traumatismo importante, a cirugía o a un
tratamiento inadecuado de osteomielitis aguda. Se caracteriza
por drenaje crónico, dolor e impotencia funcional de la
extremidad afecta. El principal agente es S. aureus,
también H. Influenzae y otros gramnegativos.
La mayoría de bacterias que
llegan al hueso son fagocitadas, pero si la zona de hueso a la
que acceden se encuentra mal vascularizada (como es el caso de la
metáfisis) los macrófagos no pueden acceder,
produciéndose un exudado inflamatorio que se acumula a
tensión entre la corteza y la médula del hueso.
Como consecuencia de la trombosis séptica de los vasos que
nutren la zona metafisaria se forma una pequeña zona de
hueso necrosado (secuestro) que es
reparado por zonas de hueso nuevo (involucro). La
infección puede extenderse hacia la médula del
hueso y/o zona epifisaria (en menores de 18 meses), pudiendo
alcanzar el espacio articular causando una
pioartrosis.

Según las formas clínicas puede
ser:
a) Agudas
b) Subagudas
c) Crónicas
d) Formas especiales
Según su patogenia, puede ser:
a) Hematógena
b) Exógena
c) Yatrogénica
Osteomielitis Aguda Hematógena
Es la infección bacteriana piógena
localizada en huesos a partir
de un área previamente infectada del organismo que se
denomina foco primario. Después del estafilococo, el
estreptococo es responsable de un 3 a 5% de los casos; el foco
primario puede estar en intestino, oído medio
o a partir de piel:
forúnculo, antrax, celulitis, etc.
Patogenia
El hueso es un tejido muy vulnerable a la
infección; los gérmenes llegan por vía
sanguínea o linfática; la lesión infecciosa
depende de la virulencia del germen y de la resistencia del
sujeto. El germen invade la metáfisis sobre todo de huesos
largos (próximas a rodilla y alejadas del codo, que son
las más fértiles), más en niños y
adolescentes;
el germen, al invadir el hueso, produce inflamación, la cual condiciona
reabsorción ósea, y las enzimas
proteolíticas y tóxicas rompen el tejido
óseo y se forma el pus; el pus retenido a tensión
se evacúa al canal medular o a la zona perióstica
formando el absceso subperióstico, el cual llega a la piel
formando una fístula; en semanas o meses hay hueso
neoformado rodeando el hueso infectado, es el llamado involucro;
el hueso infectado se descalcifica en forma irregular, y por
trombosis algunos segmentos se necrosan formándose el
secuestro que es de aspecto denso en las imágenes
radiográficas porque no participa en el metabolismo
cálcico.
En los niños rara vez llega la infección a
la articulación, por el freno que es el cartílago
metafisiario; en cadera y rodilla el compromiso articular es
más frecuente, pues el cartílago metafisiario es
intraarticular. Pueden existir focos osteomie-líticos
múltiples; la osteomielitis ocasionada por una fractura
abierta suele ser localizada más frecuentemente en
niños que niñas (proporción 4:2).
Clínica
Los síntomas varían con la edad,
virulencia del germen, localización de la
infección, intensidad, extensión, resistencia del
huésped, duración de la enfermedad y tratamiento
previo.
Los síntomas generales son como los de toda
infección aguda: malestar general, escalofríos,
fiebre,
sudoración, decaimiento, náuseas, cefalea,
etc.
Los síntomas locales están dominados por
el dolor exquisito, bien localizado, que causa espasmos
musculares y limitación de la movilidad de las articulaciones
vecinas al foco. En la práctica es difícil que
llegue de inicio, más común es que llegue en etapa
de absceso subperióstico; hay leucocitosis con
neutrofilia, VSG muy alta, anemia de tipo secundario.
La aspiración de pus de los abscesos se debe
analizar y cultivar; los hemocultivos pueden ser psotivos en 48%
de casos. Hasta los 10 ó 15 días de enfermedad, la
radiografía es negativa, la aparición de absceso es
anterior a la imagen de RX
positivo.
Osteomielitis Crónica
Hematógena
Son los enfermos que una vez pasado el período
agudo, con tratamiento o sin él, presentan
supuración piógena crónica del hueso, siendo
característica la presencia de secuestro, cavidades y
fístulas.
Clínica
Los síntomas locales inflamatorios son
reemplazados por deformidad y supuración crónica;
el dolor disminuye, excepto en caso de fractura patológica
o reactivación de la infección; se hacen evidentes
las atrofias y retardos en el crecimiento por destrucción
o alargamiento por estimulación, o angulaciones en varo o
valgo, sobre todo en rodilla; hay limitaciones de la movilidad,
fístulas, ulceraciones y raramente los
epiteliomas.
En la radiografía encontramos deformación
del contorno óseo, con esclerosis del mismo, cavidades o
geodas, presencia de secuestros, que son áreas de huesos
más densos y de contornos nítidos separados del
resto del hueso o en su interior.
Osteomielitis Crónica Primitiva – Formas
Especiales
Son casos sin sintomatología aguda aparente, con
estado general
bueno en adolescentes o personas jóvenes, en
metáfisis de fémur y tibia.
Tres formas principales:
Absceso de Brodie
Forma crónica primaria localizada, da imagen
ovoide con bordes netos y esclerosis; sus dolores suelen ser
nocturnos; localización metafisiaria; la cavidad
ósea está llena de pus, tejido de
granulación o tejido fibroso, a veces secuestros. Curan
bien con el curetaje óseo.
Osteomielitis Esclerosante de Garre
Forma crónica de baja virulencia y difusa; se
caracteriza por condensación ósea difusa de un
hueso largo y dolor neurálgico rebelde más nocturno
debido a tensión intraósea. El tratamiento consiste
en resecar la cortical esclerosada y descomprimir la
médula; no suele encontrarse pus ni nido. Tiene diagnóstico diferencial con el tumor de
Ewing.
Osteoperiostitis Albuminosa de Ollier
Absceso subperióstico de paredes engrosadas, de
contenido amarillo filante; poca sintomatología;
tratamiento quirúrgico, drenar.
Infecciones tíficas del aparato
locomotor
A nivel de huesos largos o columna; hay periostitis, es
rara y ocurre en menos de 1% de los casos tíficos.
Clínica y RX similar a la osteomielitis piógena; se
puede aislar el bacilo tífico en sangre, orina y
heces; las aglutinaciones son específicas y positivas. El
tratamiento es el de cualquier osteomielitis y el
antibiótico indicado es la cloromicetina.
Infecciones brucellósicas del aparato
locomotor
En la evolución de la Fiebre Malta se presenta
dolor en la zona sacroiliaca, columna o coxofemoral; impotencia
funcional y posición antálgica; hay fenómenos
óseos productivos y a la radiografía aumento de
densidad de
zona afectada. El diagnóstico se apoya en el antecedente y
laboratorio.
El tratamiento es a base de antibióticos adecuados y
reposo. En columna se recurre a la artrodesis, sólo en
casos rebeldes a la terapia médica.
Lues ósea
Tiene dos formas clínicas:
- Sífilis congénita: Infección
hematológica del feto a
través de madre luética; el treponema invade
todos los tejidos, las
lesiones óseas son: Osteocondritis, periostitis y
osteítis; tríada de Hutchinson. - Sífilis adquirida: Manifestación
osteoarticular de una lues secundaria y terciaria; en la
secundaria en forma de periostitis y en la terciaria como gomas
óseas, raros en la clínica diaria; el
diagnóstico lo da el laboratorio y el tratamiento
antisifilítico es efectivo.
Otra manifestación es la artropatía
neutrófica (articulación de CHARCOT) por distubio
trófico por falta de sensibilidad.
Diagnostico por Laboratorio – Reactantes de
Fase Aguda
- Útiles para el diagnóstico, seguimiento
y respuesta al tratamiento: leucocitosis, VSG (Velocidad de
Sedimentación Globular) y PCR (Proteína C
Reactiva). - En un 60% no existe leucocitosis al
diagnóstico. Una fórmula leucocitaria normal no
excluye en absoluto el diagnóstico. - La VSG, muy sensible pero poco
específica. - Se normaliza a las 3-4 semanas en casos de
osteomielitis no complicada; en un 25% de pacientes no existe
elevación de la VSG en fases iniciales. - La PCR se eleva en las primeras 8 horas, alcanza el
valor
máximo a los 2 días y se normaliza a la semana de
haber iniciado el tratamiento. Muy útil para el
seguimiento y para diferenciar formas complicadas. - Monitorización de títulos bactericidas
del suero (TBS): No se realiza de forma habitual en la
práctica diaria por su complejidad y escasa
reproductibilidad. No está indicado en todos los
pacientes, no se correlaciona con el pronóstico
pronóstico clínico y no es imprescindible para el
seguimiento clínico adecuado de los
pacientes.
Diagnostico por Imágenes
- El diagnóstico clínico debe ser precoz
para evitar el paso a la cronicidad, lo cual es determinante
desde el punto de vista pronóstico de la
infección. - Las manifestaciones clínicas (dolor, fiebre,
etc.) y las alteraciones biológicas (leucocitosis,
aumento de VSG y PCR) carecen de especificidad en las formas
agudas. - La radiografía simple es de poca ayuda en los
primeros días ya que las alteraciones óseas
iniciales no aparecen, al menos, antes de una
semana. - Las técnicas
gammagráficas detectan en los primeros días la
infección con una elevada sensibilidad (90%), pero
sólo una aceptable especificidad (73%) por la
posibilidad de falsos positivos y negativos. El 99mTc MDP es el
radiotrazador más empleado y en las fases 3 y 4 permite
diferenciar las lesiones óseas de las de partes
blandas.La asociación con citrato de 67Ga mejora la
especificidad y es útil en el control del
tratamiento. - Otras técnicas,como los leucocitos marcados
con 111In o 99mTc HMPAO, parecen ser más
específicas. - La TAC y la RM superan a las anteriores pruebas en
todos los aspectos, ya que tienen una excelente
resolución y revelan edema, daño
medular, reacción periostal, destrucción cortical
y afectación de las partes blandas, aun cuando la
radiografía simple y la gammagrafía son
todavía normales. No obstante, en la TAC es común
la degradación de la imagen por artefactos debidos al
hueso o al metal, y la RM está contraindicada cuando el
paciente porta cuerpos extraños de tipo
ferromagnético. A pesar de la disponibilidad de todo
este conjunto de técnicas diagnósticas, a veces
es necesaria la confirmación histopatológica
mediante fragmentos óseos obtenidos durante la
cirugía o por biopsia. - En el diagnóstico microbiológico, las
únicas muestras fiables para el aislamiento del agente
causal son el tejido óseo obtenido por biopsia o en el
acto quirúrgico, el material extraído por
punción de abscesos cerrados y los
hemocultivos. - Las tomas de úlceras o fístulas son a
menudo engañosas, ya que pueden corresponder a una
infección superficial o a una contaminación. El valor predictivo
positivo del exudado de la fístula es aproximadamente
del 50% y algo superior para S. aureus. La determinación
del verdadero agente causal y su sensibilidad es esencial para
hacer un correcto tratamiento antimicrobiano.


ALGORITMO DIAGNOSTICO

El diagnóstico diferencial de un niño con
dolor óseo localizado y manifestaciones sistémicas
incluye:
- Osteomielitis.
- Artritis séptica o tóxica.
- Celulitis.
- Tromboflebitis.
- Fiebre reumática aguda.
- Infarto óseo (drepanocitosis).
- Neoplasias. Al igual que en la OAH el dolor es
constante y puede existir cojera por el propio tumor o las
metástasis. Debe hacerse diagnóstico diferencial
con los siguientes tumores: osteosarcoma, tumor de Ewing,
leucemia, neuroblastoma metastático y tumor de
Wilms. - Histiocitosis X.
- Enfermedad de Perthes.
El diagnóstico se basa en las manifestaciones
clínicas, métodos de
imagen y hallazgos de laboratorio. El diagnóstico de
osteomielitis aguda se confirma por la presencia de dos de los
siguientes cuatro criterios:
- Obtención de material purulento por
aspiración del hueso y/o cultivos de hueso
positivos. - Hemocultivos, positivos en el 50-60%.
- Presencia de signos/síntomas clásicos de
osteomielitis.
Cambios por gammagrafía ósea, RMN o
radiografía, típicos de osteomielitis.
A pesar de los importantes avances logrados en el
conocimiento y manejo de la osteomielitis, aún nos
enfrentamos a un proceso con
problemas de
tratamiento y una elevada morbilidad, en particular en su forma
crónica. Las tasas de curación obtenidas son
inferiores a las de otras infecciones y no se logra esterilizar
el hueso en más del 70% de las ocasiones. El éxito
terapéutico se relación con la precocidad en el
diagnóstico, el tipo evolutivo -aguda o crónica-,
el agente causal, las características del foco de
infección, la presencia de material de implante y el
acierto en las medidas tomadas. El tratamiento de la
osteomielitis comprende el uso de antimicrobianos, cirugía
y rehabilitación física,
psíquica y social.

En el hueso normal, no existe ninguna barrera
anatómica o funcional que impida la penetración de
los antibióticos. Incluso se ha visto una estrecha
relación entre la concentración sérica y la
ósea, de tal manera que los hallazgos en el suero en la
fase de meseta pueden predecir la cantidad de antibiótico
en el hueso. Sin embargo, en la osteomielitis hay que considerar
las peculiaridades del foco de infección -acidez, isquemia
y bajo potencial "redox"- que pueden hacer fracasar la acción
beneficiosa del antibiótico.
Tampoco ha de olvidarse que estamos ante una
infección por bacterias adherentes, donde los
microorganismos producen exopolímeros altamente hidratados
-glucocálix- unidos a la membrana externa en los bacilos
gramnegativos y a los ácidos
teicoicos en los cocos grampositivos, que les permite fijarse con
firmeza a los receptores glucoproteicos de las superficies
inertes -tejidos desvitalizados, material de implante-. Los
exopolímeros forman una red o biopelícula
que preserva a las bacterias de la acción de los fagocitos
y antibióticos, y facilita su interrelación y
multiplicación, siendo en definitiva una garantía
de supervivencia.
El antibiótico seleccionado debe ser activo
frente al microorganismo causal, alcanzar concentraciones
superiores a la CMI en el foco de infección, mantenerlas
en los intervalos entre dosis y permanecer estable en el
medio.
Además, por la larga duración del
tratamiento y las dosis elevadas que se emplean hay que tener en
mente la tolerancia y la
vía de administración del propio antimicrobiano.
En situaciones de refractariedad o recurrencia ha tenido utilidad la
medición del poder
bactericida del suero en el pico y en el valle, como dato
indirecto de las cifras en el suero y para poder predecir la
respuesta al tratamiento.
Títulos ≥ a 1/16 en las formas agudas y ≥ a
1/8 en las crónicas se relacionan con buenos resultados.
El seguimiento de estas normas puede ser
suficiente para alcanzar la curación de las formas agudas,
pero no así en las crónicas que generalmente
precisan cirugía.


En el tratamiento antimicrobiano, es conocido que la
osteomielitis aguda requiere una actuación empírica
inmediata, previa recogida de muestras adecuadas, mientras que en
la crónica es preferible aguardar a conocer el
diagnóstico etiológico. Las pautas y
duración de la antibioticoterapia no están bien
establecidas, pues no hay ensayos
clínicos definitorios, aunque se acepta la necesidad de
dosis altas durante periodos prolongados – al menos seis
semanas-. Los cambios en la etiología de la osteomielitis,
el desarrollo de
resistencias y
la aparición de nuevos antibióticos, sobre todo
orales con excelente biodisponibilidad, hacen necesario la
revisión periódica de la idoneidad del
tratamiento.
En la actualidad, existe un gran número de
antibióticos para el tratamiento de la osteomielitis,
algunos de los cuales han demostrado su eficacia en
ensayos clínicos poco valorables y de escaso rigor
científico, por lo que la Infectious Disease Society of
America y la Food and Drug Administration en 1992 establecieron
una serie de condiciones que los investigadores deben seguir en
el diseño
de trabajos en este campo.
En las infecciones por S. aureus productores de
penicilinasa -90% de los aislados-, los betalactámicos han
confirmado su eficacia. Son útiles las penicilinas
isoxazólicas o asociadas a inhibidores de betalactamasas y
las cefalosporinas de 1ª y 2ª
generación.
Otras alternativas son los glucopéptidos
-vancomicina y teicoplanina-, cotrimoxazol, clindamicina -con
actividad antiadherente-, fosfomicina, ácido
fusídico, rifampicina y las fluorquinolonas -los tres
últimos nunca en monoterapia-. En S. aureus y otros
estafilococos -la mayor parte de los coagulasa negativos-
resistentes a la meticilina, recurriremos a glucopéptidos,
cotrimoxazol o a combinaciones de fluorquinolonas y
rifampicina.
La terapia secuencial iv/po es posible realizarla en la
mayoría de las ocasiones, excepto con los
glucopéptidos, aunque la presentación intramuscular
de teicoplanina y su dosis única diaria han permitido
mantener tratamientos ambulatorios prolongados con escasos
efectos adversos. La progresiva insensibilidad de los
estafilococos a los antibióticos está llevando a la
búsqueda de nuevas moléculas activas como
quinolonas -moxifloxacino, gatifloxacino, gemifloxacino, etc.-,
sinergistinas -dalfopristina/quinupristina- y oxazolidinonas
–-linezolid- entre otras, de las que no hay experiencia en
osteomielitis en la actualidad.
En el caso de los bacilos gramnegativos aerobios o
facultativos y en la formas polimicrobianas, son muy
útiles las cefalosporinas de 3ª -cefotaxima,
ceftriaxona y ceftazidima- o 4ª generación
-cefepima-, las fluorquinolonas -ciprofloxacino, ofloxacino y
pefloxacino-, las penicilinas asociadas a inhibidores de
betalactamasas – amoxicilina/clavulánico,
ampicilina/sulbactam y piperacilina/ tazobactam-, los
carbapenémicos -imipenem/cilastatina y meropenem- y
aztreonam -activo sólo frente a bacilos gramnegativos-.
Piperacilina/tazobactam, ceftazidima y cefepima tienen actividad
sobre P. aeruginosa por lo que estarían indicadas en los
usuarios de drogas por
vía parenteral, inmunodeprimidos y en las infecciones
localizadas en los pies de los diabéticos.
Los carbapenémicos también tendrían
esta indicación pero el alto coste y la corta semivida
limitan su uso. Las fluorquinolonas, sin duda alguna, han
supuesto la revolución
más importante en el tratamiento de la osteomielitis. Sus
excelentes características farmacocinéticas por
vía oral han posibilitado hacer tratamientos ambulatorios,
total o parcialmente, con buenas tasas de curación y pocos
efectos adversos.
Sin embargo, las nada despreciables tasas de resistencia
surgidas en algunos microorganismos obligan a la cautela en su
uso. Frente a S. aureus no son la primera opción y se
desaconseja la monoterapia.
En el caso de E. coli sensible se pueden emplear con
seguridad, aunque
con P. aeruginosa, donde habrá que vigilar la selección
de cepas resistentes, sería aconsejable asociar
inicialmente al menos otro antimicrobiano y cuando la
concentración de microorganismos se estime que se ha
reducido pasar a monoterapia.
Los aminoglucósidos no son recomendables en esta
situación si tenemos en cuenta que el foco de
infección tiene un pH
ácido, un potencial redox bajo y una tensión de
oxígeno
reducida, condiciones que inactivan a estos
antibióticos.
ELECCION DEL TRATAMIENTO
ANTIMICROBIANO
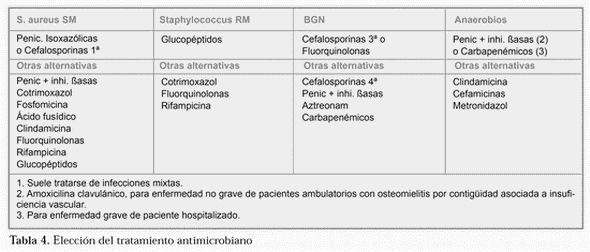
Ciertos microorganismos requieren pautas concretas.
Frente a Enterococcus una penicilina -ampicilina o piperacilina-
o un glucopéptido junto a un aminoglucósido es el
tratamiento de elección. En las infecciones por
anaerobios, la producción de betalactamasas por algunos
Bacteroides aconseja el empleo de
penicilinas asociadas a inhibidores de betalactamasas,
carbapenémicos o metronidazol, aunque clindamicina o las
cefamicinas -cefoxitina, cefmetazol- continúan siendo
útiles.
La cámara hiperbárica, también
empleada en infecciones estafilocócicas, tendría
aquí su principal indicación. Con ella se intenta
estimular la fagocitosis deteriorada por el ambiente
hipóxico y se ha mostrado tan eficaz como las
cefalosporinas.
El tratamiento de infecciones óseas
específicas como la tuberculosa, brucelar o
micótica en nada se diferencia del suyo habitual de otras
localizaciones.
La cirugía, fundamental en las formas
crónicas, va encaminada a eliminar los tejidos
desvitalizados, obliterar los espacios muertos y lograr la
estabilidad funcional. Una vez indicada, es importante saber el
momento adecuado de efectuarla y el tipo de intervención
más correcta. La rehabilitación física es
necesaria con el fin de potenciar la funcionalidad de la parte
afectada. Lo mismo ocurre con el apoyo psicológico que
persigue la prevención o curación del componente
ansiosodepresivo generado por:
- La larga hospitalización y el desarraigo
familiar, profesional y social que conlleva, - La prolongada inmovilización con complejos
sistemas de
fijación y - El pronóstico incierto de la
lesión.
El futuro pasa por las medidas antiadherentes e impedir
la creación de los biofilms o dañarlos una vez
creados. Ciertos antibióticos como las fluorquinolonas,
rifampicina y clindamicina ya han demostrado su eficacia en estos
aspectos.
La acción inmunomoduladora y deletérea
sobre el biofilm de los macrólidos, podría tener
alguna implicación terapéutica en la
osteomielitis.
Fondo Editorial de la Universidad Nacional Mayor de San Marcos. Lima
2002.- "Cirugía Ortopédica y
Traumatología"Sociedad Española de Enfermedades
Infecciosas y Microbiología
Clínica. - "Infecciones Osteoarticulares y de Partes
Blandas" - Revista Cubana de Salud
- Asociación Española de
Pediatría - Protocolos Clínicos en Enfermedades
Infecciosas del Hospital Vega Baja de Orihuela. Alicante
– España
http://factoresderiesgo.org/libro/
RAUL E. PORRAS SERNA
Estudiante de medicina
UNIVERSIDAD RICARDO PALMA – FACULTAD DE MEDICINA
HUMANA
Lima – Perú