La epilepsia mioclónica juvenil (EMJ) es un
síndrome hereditario no progresivo caracterizado por
convulsiones con sacudidas mioclónicas bilaterales,
únicas o repetitivas, de predominio en brazos. Objetivo: Analizar las
características clínicas y electroencefalográficas
en pacientes con diagnóstico de EMJ.
Metodología: Se revisaron
las historias clínicas de 13 pacientes evaluados en el
Hospital Clínico de Maracaibo entre 1990 y 1999 quienes
reunieron los criterios diagnósticos de EMJ. Analizamos los
siguientes parámetros clínicos y
electroencefalográficos: sexo, antecedentes personales
y familiares, edad de comienzo, semiología, distribución, duración
y frecuencia de las crisis, examen
neurológico, tiempo de seguimiento y
evolución. Resultados:
Nueve pacientes eran varones (69,2%) y 4 mujeres (30,8%). Tiempo
de seguimiento de 2 a 9 años (promedio 4.3 años). Las
convulsiones se iniciaron entre los 12 y 16 años, con una
edad promedio de 14 años. Las crisis fueron
tónicoclónicas generalizadas en el 100% de los casos.
Todos los pacientes presentaron sacudidas mioclónicas
matutinas y el examen neurológico resultó normal. Tres
pacientes tenían antecedentes personales de convulsiones
febriles y cuatro tenían antecedentes familiares de
epilepsia. El estudio electroencefalográfico (EEG)
interictal fue anormal en todos los casos revelando un
patrón de descargas de punta-onda o polipunta-onda con
distribución generalizada. Conclusiones: La EMJ representa
una forma de epilepsia de comienzo en la adolescencia que afecta con
mayor frecuencia a varones y está asociada a una historia familiar de convulsiones. Su curso
es benigno en la mayoría de los pacientes tratados con valproato, pero las
recidivas son comunes al descontinuar la
medicación.
Palabras clave. Adolescentes, epilepsia,
convulsiones mioclónicas, valproato.
Abstract
Juvenile myoclonic epilepsy: study on 13 Venezuelan
patients. Juvenile myoclonic epilepsy (JME) is a heritable
nonprogressive syndrome characterized by seizures and bilateral
myoclonic jerks usually of the upper extremities. Objective: To
analyze the clinical and electroencephalographic characteristics
of patients diagnosed as having JME. Methodology: We reviewed the
clinical records of 13 patients evaluated at the Hospital
Clínico, Maracaibo, between 1990 and 1999 who met diagnostic
criteria for JME. We analyzed the following clinical and
electroencephalographic parameters: sex, personal and family history, age
of onset, semiology, distribution, duration and frequency of
crises, neurological examination, time of follow-up and
evolution. Results: Nine patients were boys (69. 2%) and four
girls (30. 8%). The follow-up period was from two to nine years
(average 4.3 years). Convulsions started at age between 12 and 16
years, average 14 years. The crises were of generalized
tonic-clonic type in 100 % of cases. All patients exhibited
myoclonic jerks commonly occurring shortly after awakening, and
the neurological examination was normal. Three patients had
personal history of febrile convulsions and 4 had family history
of epilepsy. The interictal electroencephalographic (EEG) study
was considered MedULA, Revista de Facultad de
Medicina, Universidad de Los Andes. Vol. 9
Nº 1-4. 2000. (2003). Mérida. Venezuela. 21 abnormal in all
cases revealing a pattern of generalized rapid multispike and
slow wave complexes. Conclusions: JME represents a form of
epilepsy beginning in early adolescence which affects males more
often than females, associated with a family history of
convulsions. Its course is benign and seizures are controlled in
the majority of patients with valproate, but relapse is common
when medication is discontinued.
Key words. Adolescents, epilepsy, myoclonic seizures,
valproate.
La última clasificación Internacional de las
Epilepsias y Síndromes Epilépticos (1989) reconoce a la
epilepsia mioclónica juvenil (EMJ), también conocida
como síndrome de Herpin-Rabot-Janz; como una de las
epilepsias idiopáticas generalizadas relacionadas con la
edad (Anon 1). Fue descrita inicialmente por Herpin en 1867 y por
Rabot en 1899 (Delgado-Escueta, Enrile- Bacsa 1984, Janz 1985);
mientras que Janz y Christian en 1957, hacen la primera descripción detallada del
trastorno y la denominan "impulsive petit mal".
Otros términos como Epilepsia mioclónica
juvenil de Janz, y Epilepsia mioclónica, también han
sido empleados para su identificación (Delgado-Escueta,
Enrile-Bacsa 1984, Asconape, Penry 1984). Clínicamente se
caracteriza por sacudidas mioclónicas bilaterales,
únicas o repetitivas, arrítmicas, irregulares, sin
alteración de la conciencia y de predominio en los
brazos que pueden hacer caer súbitamente al paciente y las
cuales suelen aparecer habitualmente poco después del
despertar, tras el sueño insuficiente o despertar prematuro.
Las convulsiones generalizadas tónico-clónicas aparecen
después de varios años (1 a 3) del inicio de las
sacudidas mioclónicas, habitualmente entre la edad de 12 a
19 años (Haller, Resnick 1989). Al igual que en las
sacudidas mioclónicas, estas crisis frecuentemente aparecen
poco tiempo después del despertar o durante el sueño de
las primeras horas del día. Con menor frecuencia ocurren las
ausencias.
El electroencefalograma (EEG) ictal e interictal exhibe
descargas de punta-polipunta-onda de 3-5 Hz, de distribución
generalizada y frecuentemente irregular (Janz, Christian 1957,
Haller, Resnick 1989).
El desconocimiento o infravaloración de los
elementos clínicos, especialmente las sacudidas
mioclónicas y la presencia de un síndrome
epiléptico primario, genera dudas diagnósticas y
tratamientos inapropiados para este síndrome cuya respuesta
al valproato ha sido demostrada en forma
satisfactoria.
El objetivo de este trabajo es analizar las
características clínico-electroencefalográficas y
evolutivas de 13 pacientes con EMJ y enfatizar en la necesidad de
su identificación y tratamiento adecuado.
En este estudio se evaluaron las historias clínicas
de 13 pacientes que reunieron los criterios clínicos y EEG
para el diagnóstico de EMJ, atendidos en el Hospital
Clínico de Maracaibo, Venezuela, entre 1990-1999.
Se analizaron los siguientes parámetros
clínicos: sexo, antecedentes personales y familiares, edad
de comienzo, tipo de crisis, examen neurológico, tiempo de
seguimiento y evolución.
Se realizó EEG intercrítico de vigilia y
sueño a cada uno de los pacientes, ubicando los electrodos
según el Sistema Internacional 10-20. Se
analizaron la organización basal, la
topografía y la morfología.
Sexo: La muestra estuvo compuesta por 13
pacientes, 9 varones (69.2 %) y 4 mujeres (30.8%).
El tiempo de seguimiento fue de 2 a 9 años
(promedio 4.3 años).
Edad de comienzo: las convulsiones se iniciaron
entre los 12 y los 16 años, con una edad de aparición
promedio de 14 años.
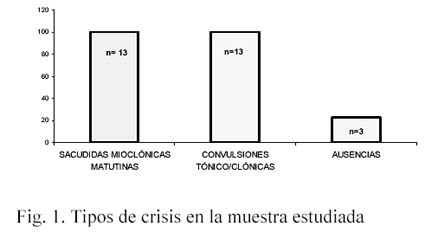
Tipos de Crisis: Todos los pacientes presentaron
sacudidas mioclónicas matutinas, sin embargo; en solo tres
casos fueron consideradas relevantes para el paciente o sus
familiares en la primera consulta neurológica. La totalidad
de la muestra presentó convulsiones
tónico-clónicas generalizadas, las cuales ocurrieron en
vigilia, especialmente al despertar y de duración breve. El
77% (n=10), presentó más de 5 crisis antes del
diagnóstico, y el 23% (n=3) presentó dos. Solo tres
pacientes manifestaron ausencias (23%). En la figura 1 se muestra
la distribución de los tipos de crisis en la muestra
descrita
Características
electroencefalográficas:
En la tabla 1 se pueden observar las
características electroencefalográficas de los
pacientes estudiados. Los EEG interictales fueron anormales en
todos los casos (100%), revelando un patrón de descargas
breves de punta-onda o polipunta-onda de alto voltaje con
distribución generalizada. En todos los casos la actividad
basal se consideró normal. Para el 23 % (n=3) la
fotoestimulación indujo la aparición de descargas
generalizadas de breve duración. En 12 pacientes (92.3%) se
señaló la deprivación de sueño como factor
desencadenante. Cinco pacientes (38.4%) relacionaron la
aparición de las crisis con estrés, tres pacientes con
la fotoestimulación y 2 con la fatiga y el alcohol (15%).

Antecedentes personales y
familiares:
Los 13 pacientes son hijos de padres no
consanguíneos y presentaron desarrollo psicomotor y examen
neurológico normal. Tres pacientes (23%) tenían
antecedentes personales de convulsiones febriles y 4 de ellos
(31%) tenían un familiar afectado con otra forma de
epilepsia (hermano, tía paterna y tío
paterno).
Evolución: Ocho pacientes (61.5%) recibieron
dos o más fármacos anticonvulsivantes diferentes al
valproato sin mejoría de las crisis, antes de su ingreso en
este protocolo de investigación. El control de las crisis fue
alcanzado en todos los pacientes (100%) después del
diagnóstico y al iniciar el tratamiento con
valproato.
Solo dos pacientes (15.3%) han tenido recidivas tras la
suspensión del fármaco en un tiempo de seguimiento de 3
años.
En adolescentes con mioclonías epilépticas
prácticamente la única alternativa diagnóstica es
la epilepsia mioclónica juvenil (EMJ) (Herranz, de las
Cuevas 1998). La edad de inicio es uno de los criterios
clínicos principales, por lo que la EMJ representa la
epilepsia primaria más frecuente entre adolescentes y
adultos (Janz, Christian 1957, Asconape, Penry 1984, Haller,
Resnick 1989). Los resultados obtenidos en esta serie de 13
pacientes demuestran claramente un predominio en varones con una
edad promedio de aparición de 14 años.
Todos los pacientes presentaron sacudidas
mioclónicas (100%), las cuales se presentaron antes del
inicio de las crisis generalizadas
tónicoclónicas.
La aparición de crisis mioclónicas en brazos,
hombros y manos, especialmente al despertar, provocan la
caída de los objetos del aseo o del desayuno. Este hecho ha
sido señalado por muchos autores y puede ser malinterpretado
por el paciente o su familia como nerviosismo, torpeza
o falta de atención (Herranz, de las
Cuevas 1998, Dreifuss 1989, Serratosa, Delgado-Escueta
1993).
Si todos los pacientes de esta serie refirieron su
presencia, solo en tres de ellos las sacudidas mioclónicas
representaron la manifestación clínica más
llamativa que motivó la consulta
neurológica.
La totalidad de los pacientes experimentaron crisis
generalizadas tónico-clónicas, de breve duración.
Estas crisis suelen producirse a continuación de una serie
de mioclonías y se desencadenan con el despertar, la
deprivación de sueño, el cansancio, la ingesta de
alcohol, el ayuno, las emociones y estrés como
ocurrió en nuestros pacientes (Herranz, de las Cuevas 1998,
Wolf, Goosses 1986).
Algunos pacientes con EMJ pueden presentar ausencias,
como fue mostrado en 3 de ellos. Estas suelen aparecer 1 a 2
años antes del inicio de las mioclonías, a los 9
años en promedio. Muchos pacientes no están conscientes
de ellas y posiblemente la mayoría de las veces pasen
desapercibidas por él y su familia (Janz 1985, Serratosa,
Delgado-Escueta 1993).
Otros hallazgos de esta serie son los antecedentes
personales de convulsiones febriles en 3 casos y el antecedente
familiar de epilepsia en 4 pacientes.
Tsuboi y Christian (1973) y Janz (1985) señalan que
de 3.3% a 8.6 % de los pacientes con EMJ presentan convulsiones
febriles. En la mayoría de los estudios, también se
advierte la asociación con el mismo u otro tipo de crisis,
historia familiar altamente positiva de epilepsia (45 al 48%) y
ausencia de factores etiológicos (Delgado-Escueta,
Enrile-Bacsal 1984, Asconape, Penry 1984, Dreifuss 1989,
Serratosa, Delgado-Escueta 1993).
Desde 1989, varios autores han reportado la
relación entre la EMJ y algunos haplotipos HLA, por lo que
se asumió la posible localización del gen de la EMJ en
los brazos cortos del cromosoma 6. EEG ANORMALES 100% (n=13)
ACTIVIDAD BASE NORMAL 100% (n=13) DESENCADENANTES
FOTOESTIMULACIÓN 23% (n=3) DEPRIVACIÓN DE SUEÑO
92,30% (n=12) STRESS 38,40% (n=5) FATIGA Y
ALCOHOL 15,40% (n=2)
Panayiotopoulos y Obeid (1989) concluyen que es una
enfermedad autosómica recesiva y
Durner et al. (1991) consideran que un mismo gen sería el
responsable de diversos tipos de epilepsia. Liu et al. (1995)
ubican el gen en 6p21.2-p11; sin embargo, varios autores
(Whitehouse et al. 1993, Sander et al. 1995, Elmslie et al. 1996)
no lograron demostrar la relación entre EMJ y marcadores
polimórficos del brazo corto del cromosoma 6, por lo que se
propone heterogeneidad genética. Finalmente en
1997, Elmslie et al. sugieren que el gen que codifica para la
subunidad a7 del receptor neuronal nicotínico, que mapea a
nivel de 15q14, contribuye a la susceptibilidad genética
para desarrollar EMJ en la mayoría de las familias
estudiadas (Elmslie et al. 1997).
En todos los casos el EEG intercrítico fue
anormal.
Brotes generalizados de punta y punta-onda rápidos
de 4 a 6 Hz, o complejos de polipunta-onda de distribución
generalizada, a menudo de duración breve, representaron las
alteraciones características. Los hallazgos
electroclínicos de nuestra serie son similares a los
reportados en la literatura (Delgado-Escueta, Enrile- Bacsal
1984, Janz, Christian 1957, Asconape, Penry 1984). Curiosamente
los tres pacientes con ausencias de nuestra serie, mostraron
sacudidas mioclónicas durante la fotoestimulación. Este
hallazgo no es específico de la EMJ, pues también ha
sido reportado en los pacientes con otros tipos de epilepsia
generalizada incluyendo las ausencias tipo "petit mal" (Janz
1985, Janz, Christian 1957, Haller, Resnick 1989).
Se destaca la excelente respuesta al tratamiento con
valproato. Ocho pacientes que recibían uno o varios
fármacos diferentes al valproato, presentaron mayor
número de crisis previo a establecerse el diagnóstico e
iniciarse el tratamiento apropiado. Sólo dos pacientes
presentaron recidivas en los 3 años de seguimiento; uno de
ellos, tras 3 años de tratamiento. Se ha señalado que
si bien casi todos los pacientes se controlan rápidamente
con valproato, el riesgo de recidiva es muy elevado
al intentar anular el tratamiento, que para muchos investigadores
debe prologarse diez o más años (Herranz, de las Cuevas
1998, Penry et al. 1989, Ferrendelli et al. 1989). Además
del seguimiento farmacológico de estos pacientes, es
recomendable revisar su calidad de vida, pues las
recidivas habitualmente se precipitan por fatiga, estrés,
incumplimiento con la medicación, ingesta de alcohol y/o
deprivación de sueño. Por otra parte, en los casos de
difícil control, o cuando se recurre a terapia con
fármacos que inducen sedación, puede haber errores
diagnósticos con las epilepsias mioclónicas
progresivas.
Ante un paciente con síndrome epiléptico
acompañado de mioclonías se recomienda realizar una
buena historia clínica que incluya la anamnesis familiar y
personal, la anamnesis detallada de las crisis epilépticas
(tipo, inicio, características, factores desencadenantes,
etc.) y la exploración neurológica completa. El
registro EEG con
estimulación luminosa intermitente a diversas frecuencias,
en vigilia, con prueba de hiperventilación durante 3 a 4
minutos y el trazado de sueño espontáneo con
deprivación de sueño facilitarán el
diagnóstico (Haller, Resnick 1989, Herranz, de las Cuevas
1998).
Habitualmente las crisis mioclónicas de la EMJ son
bilaterales y generalizadas. Suelen observarse crisis
mioclónicas en pacientes con otras formas de epilepsia
generalizada idiopática, como en la epilepsia con ausencias
y en la epilepsia con convulsiones del gran mal del despertar,
pero en estos casos, la mioclonías no son el elemento
clínico prominente (Engel 1999). El síndrome de
Lennox-Gastaut, la epilepsia mioclónico-astática y la
epilepsia con ausencias mioclónicas, debutan a menor edad,
suelen asociarse con mayor número de crisis y se
acompañan de afectación mental (Herranz, de las Cuevas
1998, Engel 1999).
Las encefalopatías progresivas o enfermedades degenerativas pueden
acompañarse de mioclonías. En estos casos,
afortunadamente poco frecuentes, se trata de niños con un desarrollo
inicialmente normal, seguido de un deterioro neurológico
progresivo acompañado de déficits neurológicos y
sensoriales, ataxia y crisis convulsivas (Lyon et al.
1996).
La EMJ constituye una condición epiléptica
propia del adolescente, caracterizada por sacudidas
mioclónicas especialmente matutinas, crisis generalizadas en
vigilia y curso benigno cuando el diagnóstico es correcto y
se instaura un tratamiento adecuado. EL examen neurológico
es habitualmente normal y los hallazgos
electroencefalográficos son específicos. Cuando un
adolescente presenta crisis mioclónicas y reúne las
características enunciadas conviene pensar en EMJ. El
tratamiento adecuado con valproato asegura el control de las
crisis, aunque a veces es necesario mantener la medicación
durante años habida cuenta de las frecuentes recidivas tras
la suspensión. Finalmente, para orientar el diagnóstico
de este trastorno es necesario tener presente que el paciente
puede obviar las sacudidas mioclónicas; no obstante, su
existencia sólo puede ser demostrada con una historia
clínica detallada y específica.
Anonymous. 1989. Commission on Classification and
Terminology of the International League against Epilepsy.
Proposal for Revised Classification of Epilepsy and Epileptic
Syndrome. Epilepsia 30: 389- 399.
Asconape J, Penry JK. 1984. Some clinical and EEG
aspects of benign juvenile myoclonicepilepsy. Epilepsia 25:
108-114.
Delgado-Escueta AV, Enrile-Bacsal F. 1984. Juvenile
myoclonic epilepsy of Janz. Neurology 34: 285-294.
Dreifuss FE. 1989. Juvenile myoclonic epilepsy:
Characteristics of a primary generalized epilepsy. Epilepsia 30
(suppl. 4): S1-S7.
Durner M, Sander T, Greenberg DA, Johnson K,
Beck-Mannagetta G, Janz D. 1991. Localization of idiopathic
generalized epilepsy om chromosome 6p in Families of juvenile
myoclonic epilepsy
patients. Neurology 41: 1651-1655.
Elmslie FV, Rees M, Williamson MP, Kerr M, Kjeldsen M,
et al. 1997. Genetic mapping of a mayor susceptibility locus for
juvenile myoclonic epilepsy on chromosome 15q. Hum Mol Genet 6:
1329-1334.
Elmslie FV, Williamson MP, Rees M, Kerr M, Kjeldsen M et
al. 1996. Linkage analysis of juvenile myoclonic epilepsy and
microsatellite loci spanning 61 cM of human chromosome 6p in 19
nuclear pedigrees provides no evidence for a susceptibility locus
in this region. Am J Hum Genet 59: 653-663.
Engel J. 1999. Juvenile myoclonic epilepsy. Neurobase. 3
ed. Arbor Publishing Corp. Ferrendelli JA, Delgado-Escueta AV,
Dreifuss F, Penry JK. 1989. Juvenile myoclonic epilepsy: panel
discussion. Epilepsia 30 (Suppl. 4):S24-27.
Haller J, Resnick TJ. 1989. Juvenile Myoclonic Epilepsy
Easily Treated and Easily Overlooked. Intern Pediatr 4:
207-211.
Herranz JL, de las Cuevas I. 1998. Enfoque
diagnóstico del niño con crisis mioclónicas
aisladas o asociadas a otros tipos de crisis. Rev Neurol 26:
301-307.
Janz D. 1985. Epilepsy with impulsive petit mal
(Juvenile Myoclonic Epilepsy). Acta Neurol Scand 72: 449-459.
Janz D, Christian W. 1957. Impulsive petit mal. Deutsche
Zeitschrift fur Nervenheilkunde. 176: 346-386.
Liu AW, Delgado-Escueta AV, Serratosa JM, Alonso ME,
Medina MT et al. 1995. Juvenile myoclonic epilepsy locus in
chromosome 6p21.2- p11: linkage to convulsions and
electroencephalography trait. Am J Hum Genet
57:368-581.
Lyon G, Adams RD, Kolodny EH. 1996. Neurology of
Hereditary Metabolic Diseases of Children. 2 ed. McGraw-Hill. New
York.
Panayiotopoulos C, Obeid T. 1989. Juvenile myoclonic
epilepsy: an autosomal recessive disease. Ann Neurol 25:
440-443.
Penry JK, Dean JC, Riela AR. 1989. Juvenile myoclonic
epilepsy: long-term response to therapy. Epilepsia 30:
S19-23.
Sander T, Hildmann T, Janz D, Wienker T, Neitzel H,
Bianchi A, et al. 1995. The phenotypic spectrum related to the
human epilepsy susceptibility gene 'EJM1'.Ann Neurol
38:210-217.
Serratosa JM, Delgado-Escueta AV. 1993. Juvenile
myoclonic epilepsy. En: Wyllie E. (Ed.) The treatment of
epilepsy: Principles and practice. Lea& Febiger.
Philadelphia. pp 552-570.
Tsuboi T, Christian W. 1973. On the genetics of the
primary generalized epilepsy with sporadic myoclonias of
impulsive petit mal type.
(*) Trabajo presentado en el VII Congreso Venezolano de
Medicina Física y
Rehabilitación. Mérida. Venezuela. 2002.
Joaquín A. Peña (1)
En MedULA, Revista de Facultad de Medicina, Universidad
de Los Andes. Vol. 9 Nº 1-4. 2000. (2003). Mérida.
Venezuela.
Cecilia Montiel-Nava1, Sandra González F.2, Freda
Hernández1, Enoe Medrano.
(1) Postgrado de Neurología Pediátrica.
Hospital Universitario de Maracaibo. Facultad de Medicina.
Universidad del Zulia. Maracaibo. Venezuela. (2) Unidad de
Genética Médica. Hospital Universitario de Maracaibo.
Maracaibo. Venezuela.
Correspondencia: Joaquín A. Peña/Cecilia
Montiel. Apartado Postal 10171-Bella Vista. Maracaibo, Estado Zulia. Venezuela. Tel:
261-7412509.
