- Resumen
- Elementos del Subnivel
S - Elementos del
Subnivel P - Elementos del
Subnivel D - Elementos del
Subnivel F - Conclusión
- Bibliografía
COMPORTAMIENTOS QUÍMICOS,
FÍSICOS Y APLICACIÓN EN LA VIDA DIARIA DE LOS
ELEMENTOS DE LOS DIFERENTES BLOQUES EN LA TABLA PERIÓDICA
(s – p – d – f )
Resumen
En esta monografía se presentan las propiedades
físicas (estado de la
materia, punto
de ebullición, etc); las propiades químicas
(configuración electrónica, estado de oxidación,
etc); y la aplicación que se le da en la vida diaria a
cada uno de los elementos de la tabla
periódica hasta el 103 (en número
atómico).
La monografía
está clasificada en 4 capítulos, uno por cada uno
de los bloques de subniveles (s, p, d, f) en la tabla
periódica.
INTRODUCCIÓN
En este trabajo se
presenta una monografía sobre todos los elementos de la
tabla periódica, divididos en los cuatro bloques de
subniveles (s – p – d – f).
Se presenta una breve información sobre cada elemento, junto a
sus propiedades químicas (número
atómico, estado de oxidación, electronegatividad,
radio
covalente, radio iónico, radio atómico,
configuración electrónica y potencial de
ionización); sus propiedades físicas (estado
de la materia, punto de fusión,
punto de ebullición, entalpía de
vaporización y fusión, presión de
vapor y velocidad del
sonido); y su
aplicación en la vida cotidiana (que usos tiene en
la industria,
hogar, medicina,
etc).
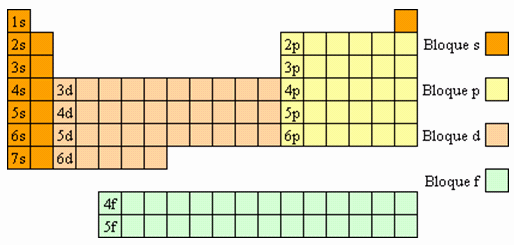
En esta ilustración podemos observar como se
dividen los bloques de la tabla periódica para la mejor
comprensión de este trabajo.
CAPÍTULO
1: COMPORTAMIENTOS FÍSICOS Y QUÍMICOS,
APLICACIÓN EN LA VIDA DIARIA DE LOS ELEMENTOS DEL SUBNIVEL
"S"
Los elementos del bloque s (del inglés
sharp) son aquellos situados en los grupos 1 y 2 de
la tabla periódica de los elementos. En estos elementos el
nivel energético más externo corresponde a
orbitales s.
El hidrógeno es un elemento químico
representado por el símbolo H y con un número
atómico de 1. En condiciones normales de
presión y temperatura, es un gas
diatómico (H2) incoloro, inodoro,
insípido, no metálico y altamente inflamable.
Con una masa atómica de 1,00794(7) u, el
hidrógeno es el elemento químico más
ligero y es, también, el elemento más
abundante, constituyendo aproximadamente el 75% de la materia
del universo.
Número Atómico
1
Estado de Oxidación
+1
Electronegatividad
2, 1
Radio Covalente
(Å)0,37
Radio Iónico
(Å)2,08
Radio Atómico
(Å)–
Configuración
Electrónica1s1
Primer Potencial de Ionización
(eV)13,65
Masa Atómica
(g/ml)1,00797
- Propiedades Químicas del
HidrógenoEstado de la Materia
Gas
Punto de Fusión
14,025 K
Punto de Ebullición
20,268 K
Punto de Inflamabilidad
255 K
Punto de Autoignición
773 – 844
KEntalpía de
Vaporización0,44936
kJ-mol-1Entalpía de
Fusión0,05868
kJ-mol-1Presión de Vapor
209 Pa a 23 K
Punto Triple
13,8033 K ;
7,042×103 PaPunto Crítico
23,97 K ;
1,293×106 PaVelocidad del Sonido
1270 mxs-1 a
298,15 KSolubilidad en Agua
1,7 mgxl-1 a
293,15 KViscosidad
8,6×10-5 P a
273,15 KTensión Superficial
2,438×10-3
N·m-1 a 18,65 K - Propiedades Físicas del
Hidrógeno - Aplicación en la Vida Diaria del
Hidrógeno
- El Hidrógeno
- Se requiere para la síntesis
de amoníaco. - Se requiere para el procesamiento de combustibles
fósiles. - Participa en la manufactura
del ácido clorhídrico. - Participa como agente reductor para minerales
metálicos. - Se emplea como refrigerante en generadores
eléctricos en las estaciones
eléctricas. - 2 moléculas de hidrógeno + 1
molécula de oxígeno forman el
agua.
Página siguiente  |

