La infección se inicia en la zona de la
máxima actividad fisiológica
del hueso; por eso, en los huesos largos la
infección se desarrolla e inicia en la región
yuxtaepifisaria situada entre la diáfisis y cada una de
las dos extremidades del hueso; efectivamente, en estas zonas se
encuentran los cartílagos de crecimiento, gracias a los
cuales el hueso se desarrolla en longitud durante la época
del desarrollo, en
la que, como hemos indicado, se presenta con más
frecuencia la osteomielitis.
También es innegable que las contusiones intensas
sufridas por un hueso favorecen el desarrollo de los microbios
sobre la zona del hueso mortificada por el traumatismo; tan
verdad es esto, que esta enfermedad suelen sufrirla con
más frecuencia los rapaces más díscolos y
vivos que sufren caídas, contusiones y distorsiones.
Las lesiones producidas en el tejido óseo por los
microbios -procedentes de la sangre e
implantados en el hueso con la colaboración o no de un
trauma – son debidas, en parte, a las toxinas producidas por los
microbios, y en parte también a la falta de nutrición del hueso
por la trombosis de los vasos sanguíneos que aportan el
pábulo nutricio a la zona del tejido óseo afectado
por la infección. Es decir, el microbio asaltante no
sólo ataca al hueso directamente por medio de sus
mortíferas toxinas, sino que provoca la
interrupción de las vías de nutrición
sanguíneas locales a través de las cuales el tejido
óseo se nutre y mantiene su vitalidad y capacidad de
resistencia; el
microbio se comporta como el general que al atacar al enemigo con
sus tropas, además de la acción
directa de éstas (toxinas microbianas en la
comparación), lleva a efecto la destrucción de las
vías de aprovisionamiento (vasos sanguíneos
en la comparación) a través de los cuales el
enemigo recibe armas,
municiones, o sea, los medios
para resistir el ataque frontal.
La zona del hueso lesionado directamente por las toxinas
microbianas y por la falta de pábulo nutricio provocada
por la oclusión trombótica vascular, empieza a
supurar y se necrosa; la zona ósea circundante que se
afecta con menos intensidad por la inflamación, logra sobrevivir y constituye
el estímulo a partir del cual se origina la
proliferación de nuevo tejido óseo que sirve para
circunscribir y aislar la zona de hueso muerta e
irrecuperable.
Volviendo a la comparación anterior, el hueso se
comporta como aquel ejército que habiendo sufrido un
descalabro en sus líneas defensivas por un violento ataque
del enemigo, circunscribe la brecha abierta, rodeándola de
tropas frescas y vigorosas bien armadas (tejido óseo de
nueva producción). En la formación de este
nuevo tejido óseo toman parte también la capa
interna del periostio (membrana que circunda el hueso) y la
médula ósea interna, que también se ha
irritado e inflamado por la infección.
Por lo tanto, en la inflamación osteomielítica
desarrollada encontraremos las siguientes zonas:
a) Una zona central
más o menos amplia, constituida por tejido óseo
deshecho y reblandecido por la supuración y la necrosis:
se denomina secuestro
óseo.
b) Una barrera
periférica más o menos ancha, constituida por
tejido óseo, compacto, de nueva formación; se le ha
llamado " caja de muerto" porque aisla y encierra el tejido
muerto del secuestro, tal como la caja encierra al
cadáver.
Pero si el cirujano tarda en practicar la intervención
de secuestrectomía (extirpación del secuestro, el
pus de éste, sobre todo si es superficial, acaba por
labrarse una salida hacia los tejidos blandos
circundantes y luego hacia el exterior; en algunas ocasiones se
evacúa en la cavidad de una articulación vecina,
produciendo una piartrosis, es decir, una colección de pus
intraarticular.
Hasta ahora hemos descrito la evolución más corriente de la
osteomielitis, es decir, la que provoca la supuración y la
necrosis circunscrita; pero existen también casos
más raros en los que la infección, por ser muy
leve, se resuelve sin formación de pus y de necrosis; en
otros, es tan grave que se difunde con gran rapidez por casi todo
el hueso a consecuencia de la extrema virulencia del ataque
microbiano y la gran debilidad de la resistencia ósea.
En estos casos, hipertóxicos graves, el hueso queda
casi completamente destruido en su zona diafisaria, y con gran
facilidad se fractura espontáneamente al más
mínimo traumatismo porque está casi completamente
reducido a un saco de pus rodeado de una capa sutil de hueso; las
dos cabezas o extremidades óseas (epífisis, que en
general se afectan menos) acaban separándose de la
diáfisis, que se destruye casi completamente.
La iniciación de la enfermedad es brusca y violenta: al
niño le aqueja de repente una fiebre elevada
con intensos escalofríos, grave malestar general,
vómito,
abatimiento, dolor de cabeza, somnolencia e incluso delirio. Los
padres presagian inmediatamente una grave infección; la
naturaleza y
la localización de la infección se aclaran
únicamente cuando el niño empieza a lamentarse de
un dolor vivísimo y continuo en una pierna, en un muslo o
en un brazo, según las diversas localizaciones.
Mediante la inspección de la extremidad dolorosa, el
médico nota durante los primeros días una
impotencia funcional de la extremidad, es decir, la imposibilidad
de moverla por el gran dolor que se exacerba al más
mínimo movimiento y
presión
local; más tarde la extremidad se hincha, enrojece y se
calienta en la zona del hueso lesionado por la infección;
posteriormente se produce el reblandecimiento de la
tumefacción por la fluidificación purulenta interna
que constituye el preludio de la abertura de una fístula,
a través de la cual fluye el pus mezclado con
pequeños fragmentos del hueso destruido. Introduciendo por
el conducto fistuloso un estilete esterilizado, se nota en el
fondo la resistencia típica del hueso muerto (secuestro)
que alimenta el flujo purulento, y a partir del cual se
desprenden los fragmentos óseos que muestran los
síntomas evidentes de la erosión
destructiva por los bordes irregulares y recortados que
presentan.
El término de la enfermedad está ligado, como es
lógico, a la intensidad, la gravedad y la difusión
del proceso
osteomielítico, que depende estrictamente de la virulencia
del microbio invasor (el estafilococo áureo es el
más virulento) y de la capacidad de las fuerzas de
resistencia antiinfecciosa del organismo asaltado. En las formas
hipertóxicas, el niño puede morir en los primeros
días por la extrema agudeza de la infección
septicémica general (fiebre altísima, delirio
continuo, etc.).
El tratamiento se dirige, en primer término, contra la
infección septicémica general, mediante la
administración de penicilina (u otros
antibióticos como la aureomicina y la terramicina) o de
sulfamidas; en la actualidad se usan poco las vacunas y los
sueros específicos (antiestafilocócicos,
antiestreptocócicos, etc.).
De esta forma, atenuando o dominando la agudeza de la
infección general son también menos graves y
extensas las lesiones óseas locales. En el hueso lesionado
el cirujano debe intervenir cuando se ha formado el pus, sin
tener en cuenta que se haya abierto camino espontáneamente
al exterior mediante una fístula. Interviniendo
precozmente se consiguen las siguientes ventajas:
eliminación del estado de
tensión local, con la consiguiente desaparición o
notable disminución de los dolores; evacuación
rápida del pus apenas formado, y la consiguiente
declinación de la fiebre y de otros síntomas de
infección septicémica general, y la posibilidad de
limitar las destrucciones óseas locales.
La intervención
quirúrgica -que se practica con
narcosis- consiste en la incisión de los tejidos blandos y
trepanación del hueso lesionado, extirpando toda la zona
de tejido irreparablemente destruida (secuestro óseo); si
es necesario se llega (en profundidad) hasta el conducto medular
que recorre interiormente el hueso en sentido longitudinal. Se
deja durante bastantes días bien abierta la brecha
practicada, al objeto de que fluya el pus y los fragmentos
óseos destruidos. Para dominar con más facilidad la
infección y la destrucción local, se puede
introducir penicilina u otro antibiótico en el espacio
vacío que queda en el hueso.
En un segundo tiempo -unos
meses después de la completa curación del proceso
osteomielítico- se puede intervenir de nuevo (con
finalidad ortopédica), al objeto de tratar las
deformaciones residuales locales y recuperar la función y
la estética de la extremidad
lesionada.
Algunas palabras sobre la osteomielitis crónica. Puede
surgir en forma crónica desde el principio o hacerse
crónica a partir de un proceso osteomielítico agudo
precedente. La osteomielitis crónica " ab initio"
está provocada o por el vigor de las fuerzas
orgánicas defensivas o por la escasa virulencia de los
microbios invasores, los cuales, localizándose en la
médula ósea, provocan una inflamación que no
tiene tendencia a la difusión periférica, pero
forman un absceso perimedular pequeño y bien circunscrito
que puede durar algunos años sin producir dolores ni
trastornos graves.
La osteomielitis crónica consecutiva a la forma aguda
se presenta cuando la intervención quirúrgica no ha
limpiado completamente el hueso, dejando algunas pequeñas
cavidades intraóseas, que pueden durar indefinidamente,
reagudizándose en un momento dado y dando lugar a una
osteomielitis aguda. De aquí la necesidad de que la
intervención quirúrgica en el hueso sea,
además de precoz, amplia y radical, al objeto de no dejar
pequeñas cámaras purulentas.
La osteomielitis crónica -tanto una forma como la otra-
produce una alteración de la estructura del
hueso, que en ciertos puntos provoca intensos procesos de
reabsorción y rarefacción del tejido
(osteítis rarefaciente), y en otros, en cambio,
procesos de condensación y espesamiento (osteítis
condensante o hiperplástica). En la zona de
osteítis rarefaciente, la resistencia del hueso a las
contusiones está disminuida y las fracturas se producen
con facilidad.
Osteomielitis agudas secundarias a infecciones generales y
locales. – Hasta ahora se ha tratado de las osteomielitis –
agudas y crónicas – primitivas, es decir, que surgen en
plena salud y no
durante o poco después de las infecciones de orden general
o local, provocadas por microbios (generalmente el estafilococo
áureo) procedentes directamente del exterior, y penetrados
en la sangre a través de una herida insignificante o una
rozadura que ha pasado desapercibida.
Pero existen también osteomielitis agudas
secundarias a otras infecciones generales y locales
preexistentes, en las que el proceso osteomielítico
representa una localización infecciosa
secundaria. En otras palabras: los
microbios responsables de la osteomielitis primitiva
o primaria pro vienen directamente del exterior y, por lo tanto
no han producido ningún foco de infección local o
general en el organismo, que resulta invadido primariamente por
el proceso osteomielítico, en cambio, los microbios
responsables de la osteomielitis secundaria ya
existen en el organismo, provocando una
infección general o local antes de
atacar al hueso y producir la
aparición di una osteomielitis, la cual
representa una localización infecciosa
secundaria del mismo microbio (o de otro
asociado). Pertenecen a esta categoría
de osteomielitis agudas
secundarias las que se presentan
después de las enfermedades
infecciosas generales (tifus, paratifus,
fiebre de Malta, pulmonía, escarlatina,
sarampión, etc.) o de focos sépticos locales
(forúnculos, ántrax, abscesos,
anginas, otitis, etc.):
El cuadro anatomopatológico y clínico de estas
osteomielitis secundarias no
difiere sustancialmente del cuadro de las
osteomielitis primitivas descritas en el capítulo
precedente; lo mismo ocurre con el tratamiento general.
Dignas de mención son:
1) La
osteomielitis tífica o paratífica, que surge en el
curso de un tifus o paratifus, o poco después de su
resolución; se localiza preferentemente en el
fémur, en la tibia, en una costilla, en una
vértebra, etc., y está provocada por el propio
bacilo del tifus o paratifus, que se implanta en dichos huesos
aprovechando un " locus minoris resistentiae" causado por una
fuerte contusión en el hueso.
2) La
osteomielitis por el micrococo melitense, que aparece como una
complicación bastante frecuente de la fiebre de Malta de
curso prolongado; el micrococo melitense responsable de la
infección se desarrolla preferentemente en una
vértebra o en una costilla, aunque tampoco respeta por
completo los huesos de las extremidades inferiores
(fémur, tibia, etc.).
3) La
osteomielitis neumocócica, que aparece en el curso de una
pulmonía (especialmente en los niños)
o poco después de su resolución; está
provocada por el mismo neumococo responsable de la
infección pulmonar, el cual se implanta generalmente en la
extremidad superior del fémur cerca de la
articulación de la cadera, la cual, en algunas ocasiones,
se ve envuelta en el proceso infeccioso.
Osteítis tuberculosa (o tuberculosis
ósea)
La infección del hueso por los bacilos tuberculosos se
presenta con mayor frecuencia en la edad juvenil y es siempre
secundaria a otras localizaciones tuberculosas -ocultas o
manifiestas, larvadas o en actividad- de nuestro organismo; en
efecto, en las osteítis tuberculosas clínicamente
primitivas, en las cuales el foco óseo parece ser la
única localización tuberculosa de nuestro
organismo, se encuentra siempre una
lesión tuberculosa que debe considerarse como el
foco primitivo, a partir del cual emigran y se implantan en el
hueso; en muchas ocasiones este foco tuberculoso primitivo
está apagado e inactivo o cursa en forma crónica,
habiendo pasado desapercibido en su fase florida por la gran
benignidad de su curso. Pero el hueso puede recibir el bacilo
tuberculoso no sólo por vía sanguínea, sino
también por contigüidad (vecindad) de un foco
tuberculoso articular (artritis tuberculosa) o por
vía linfática.
En algunas ocasiones un trauma (contusión fuerte,
distorsión violenta, etc.) favorece el desarrollo de los
bacilos tuberculosos en el hueso ni crear un " locus minoris
resistentiae" sobre el que se implantan con facilidad dichos
bacilos. En otras ocasiones -con más frecuencia- el
traumatismo despierta o activa un foco tuberculoso preexistente
absolutamente inactivo desde hace mucho tiempo y
clínicamente curado.
De los diversos huesos de nuestro esqueleto, los que se
afectan con más frecuencia por la tuberculosis son las
vértebras, las costillas, los pequeños del carpo
(en la mano) y del tarso (en el pie), las epífisis de los
huesos largos de las extremidades; muy rara es, en cambio, la
tuberculosis de los huesos de la calota craneal y del esqueleto
facial.
La primera localización de los bacilos tuberculosos en
el hueso es la médula; este foco medular inicial se
amplía progresivamente por invasión del tejido
óseo vecino, siguiendo una evolución
preferentemente exudativo-caseosa en algunas ocasiones y
productivo-fungosa en otras. Por eso se distinguen – desde el
punto de vista anatomo-patológico – dos grandes formas de
tuberculosis ósea: la exudativo-caseosa y la
productivo-fungosa.
La tuberculosis ósea exudativo-caseosa – que se
desarrolla preferentemente en los niños con un terreno
fuertemente receptivo a la infección tuberculosa – se
inicia en forma de exudación serofibrinocelular que
evoluciona después con mayor o menor rapidez como todos
los exudados tuberculosos, cualquiera que sea su
localización: es la necrosis caseosa (ver Necrosis) que
destruye todo el tejido óseo del foco, reduciéndolo
a una especie de masa informe, la cual,
por sus caracteres de sequedad y friabilidad y colorido
ligeramente amarillo, recuerda el queso, de donde procede el
adjetivo de " caseosa" que recibe la necrosis de este tejido,
típica de la infección tuberculosa.
La tuberculosis ósea productivo-fungosa se caracteriza
por la formación de tejido de granulación
constituido por los típicos Tubérculos, que
infiltran y destruyen las trabéculas óseas para
terminar provocando la necrosis caseosa que hemos descrito
anteriormente.
Posteriormente la masa necrótico-caseosa formada por
las dos formas de osteítis tuberculosas descritas, puede
sufrir -por la acción de las enzimas
producidas por los leucocitos sanguíneos- un proceso de
colicuación, es decir, de reblandecimiento, de
fluidificación con formación del
característico pus grisáceo tuberculoso, que, por
lo tanto, no es más que la masa caseosa reblandecida,
fluidificada, con pequeños trozos de tejido
necrótico, algunos leucocitos y bacilos tuberculosos.
Cuando el proceso desintegrativo llega a este punto y el
tejido óseo ha sufrido la destrucción y el
esfacelo, se forma en el interior del propio tejido una cavidad
más o menos amplia, llena de pus y con las paredes
anfractuosas tapizadas por muchos tubérculos que
continúan la erosión del tejido óseo
circundante, ensanchando cada vez más los contornos
periféricos de la propia cavidad.
Este es el cuadro de la caries tuberculosa, caracterizada por
la cavidad intraósea purulenta, la cual por la progresiva
destrucción periférica alcanza la superficie
externa del hueso, perforando la membrana del periostio y
abriéndose camino hacia los tejidos blandos y carnosos de
la vecindad. Se forma entonces el absceso frío o
tuberculoso, que no es más que una bolsa de pus
amarillenta en el seno de los tejidos blandos perióseos;
este absceso se denomina osifluente, por su origen, a partir de
la cavidad excavada en el hueso, con la que mantiene comunicación, y a partir de la cual se
alimenta de pus si el proceso destructivo de caries no se detiene
y continúa destruyendo progresivamente el tejido
óseo.
Este absceso frío osifluente se labra un camino hacia
la superficie corporal, a lo largo de las vainas perivasculares y
de los intersticios musculares; cuando el absceso alcanza el
tejido celular subcutáneo aparece una tumefacción
más o menos voluminosa, blanda y recubierta de piel, no
enrojecida ni caliente, que acaba erosionando la piel hasta que
vierte al exterior su típico y característico pus
grisáceo. Se forma así la fístula, es decir,
un trayecto largo, irregular y tortuoso, excavado en los tejidos
blandos, que partiendo del hueso en la profundidad elimina al
exterior el pus de origen óseo. Los abscesos fríos
alimentados por la tuberculosis de las vértebras lumbares
– descrita en la palabra Pott (MAL DE)- pueden superficializarse
y vaciarse mediante una fístula a nivel de la zona
más elevada e interna del muslo.
Después de esta sucinta descripción del proceso
anatomopatológico de la osteítis tuberculosa
refiriendo las sucesivas fases de tuberculosis exudativo-caseosa
o productivo-fungosa, de caries ósea tuberculosa, de
absceso frío osifluente y de fístula tuberculosa
por la cual se elimina el pus del foco óseo, pasaremos a
describir la sintomatología de la
osteítis tuberculosa.
La iniciación es lenta, insidiosa y subrepticia: el
paciente advierte localmente un dolor sordo y continuo, que se
hace más intenso de noche y por la palpación o
compresión local. Más tarde, en la zona lesionada
empieza a elevarse una tumefacción blanda y pastosa,
cubierta por la piel de aspecto normal (no enrojecida ni
caliente).
Este abultamiento está producido por el absceso
frío que se va superficializando progresivamente, hasta
abrirse al exterior mediante una fístula que da salida
continuamente al pus grisáceo mantenido por la caries
tuberculosa del hueso. Los bordes de la abertura externa de la
fístula son irregulares, recortados, fungosos, no
turgentes ni enrojecidos como en el absceso caliente, sino
más bien lacios y violáceos. La fístula no
se cierra casi nunca espontáneamente, y con el tiempo
puede originar una infección piógena secundaria si
los tratamientos locales no son frecuentes y escrupulosos. Al
abrirse el absceso frío mediante la fístula,
desaparece o por lo menos se atenúa mucho el dolor.
Esta es la sintomatología y el curso de cualquier
osteítis tuberculosa prescindiendo de su
localización particular. Para la descripción de las
diversas localizaciones, nos remitimos a Pott (ENFERMEDAD DE),
para la tuberculosis vertebral; a Espina ventosa, para la
tuberculosis de los meta-carpianos, metatarsianos y falanges; a
COXITIS TUBERCULOSA, para la tuberculosis osteoarticular de la
cadera; para la tuberculosis osteoarticular de la rodilla, ver
Osteoartritis tuberculosa de la rodilla.
El diagnóstico de la tuberculosis ósea
puede presentar -sobre todo en la fase inicial- ciertas
dificultades en relación con el diagnóstico
diferencial con la osteomielitis subaguda y crónica, con
la sífilis
ósea y con los tumores óseos. Pero con el concurso
de los síntomas clínicos (curso crónico,
tórpido, indoloro de la lesión, hallazgo eventual
de lesiones tuberculosas en actividad, en los pulmones o en otros
órganos, etc.) y del examen radiológico
(diferenciando el aspecto de la lesión ósea
según se trate de tuberculosis, osteomielitis
crónica, sífilis o tumor), es posible lograr un
diagnóstico de certeza.
El tratamiento consiste en colocar en reposo la parte enferma
durante un tiempo bastante prolongado, mediante la
inmovilización con vendaje de yeso u otro medio de
contención. Desde el punto de vista general, está
indicada la alimentación abundante, la cura de sol
(helioterapía) y las localidades marítimas.
El tratamiento con estreptomicina, cicloserina, viomicina,
piracínamida y con hidrazida del ácido
isonicotínico y PAS en la tuberculosis osteoarticular
tiene una eficacia muy
apreciable. Si es necesario, se llegará a la
intervención quirúrgica del hueso enfermo; la
naturaleza de esta intervención varía según
el hueso lesionado y en relación con el grado de gravedad
que alcance la lesión. Los abscesos fríos que se
superficializan se tratan -antes de que se abran
espontáneamente, formando fístulas que se cierran
con dificultad- mediante la punción evacuadora del pus y
la introducción de estreptomicina o de
líquidos modificadores (soluciones
yodoyoduradas).
Osteítis sifilítica o luética
(sífilis ósea). -Las lesiones sifilíticas de
los huesos pueden estar provocadas por la sífilis
congénita y por la sífilis adquirida
después del nacimiento.
La forma principal de la sífilis ósea
congénita es la osteocondritis sifilítica (que se
encuentra en casi todos los fetos sifilíticos de
más de 6 meses de gestación), la cual se localiza
tanto en las extremidades anteriores de las costillas como en los
huesos largos de las extremidades a nivel de la región
yuxtaepifisaria donde está situado el cartílago de
crecimiento del hueso.
El tejido específico de granulación que
caracteriza esta osteocondritis sifilítica
congénita ejerce una acción osteolítica (es
decir, de disolución y reabsorción del tejido
óseo) sobre las trabéculas óseas y
cartilaginosas de la región yuxtaepifisaria, que separa la
diáfisis de los huesos largos, de las extremidades o
epífisis; la interrupción completa de este
armazón produce el desprendimiento epifisario, es decir,
la separación de las epífisis del resto del hueso,
aunque no se produce ningún desplazamiento entre los
muñones óseos porque el periostio periférico
está reforzado y engrosado por un proceso de periostitis
luética, y además se forma una ganga de fibrina y
de detritus óseos y cartilaginosos interpuesta entre la
epífisis y el hueso, que impide también dicho
desplazamiento. Facilita la producción de este
desprendimiento epifisario, que a veces se presenta
espontáneamente, la tracción ejercida por el
obstetra sobre el brazo o la pierna del recién nacido en
el curso de un parto
laborioso.
Otras formas de sífilis ósea congénita
son:
a) La osteomielitis
diafisaria, caracterizada por la formación de un tejido
gomoso de granulación que provoca graves deformaciones en
el desarrollo ulterior del hueso por los procesos
osteoclásticos (destructivos) que se producen en algunos
puntos y los osteoblásticos.
b) La periostitis, que se
presenta en los huesos planos y en la zona central
(diáfisis) de los huesos largos; consiste en el
depósito de concreciones óseas de espesor variable
a nivel de la superficie abollonada que circunda al hueso,
formando un verdadero manguito.
Las deformaciones óseas que revelan la existencia de
una sífilis congénita son las siguientes:
- la " tibia en sable" , es decir, deformada
en forma de hoja de sable;
- la " frente olímpica" , es decir,
muy elevada por los procesos hiperostósicos del hueso
frontal;
- la " frente en quilla" , es decir,
propulsando hacia delante, como la quilla de una nave; esta
deformación también está provocada por la
hiperóstosis del hueso frontal;
- el " caput natiforme" , caracterizado por
el hundimiento sito entre las prominencias frontales y las
parietales muy desarrolladas de la calota craneal;
- la " nariz en silla de montar" , es decir,
deprimida y hundida por su parte superior;
- el " paladar ojival" ; etc.
Es preciso indicar que el raquitismo puede también
provocar las deformaciones anteriores.
Describiremos a continuación las lesiones óseas
producidas por la sífilis adquirida después del
nacimiento; pertenecen al
período terciario de la
infección sifilítica. Desde el
punto de vista anatomopatológico se
distinguen las siguientes formas: periostitis no gomosa,
osteítis no gomosa, Ottioperiostitis gomosa, osteomielitis
gomosa. Los GOMAS, que caracterizan estas dos últimas
formas, son la consecuencia de un proceso de granulación
específica luética; estos gomas, después de
haber corroído el tejido óseo, pueden sufrir las
siguientes evoluciones:
-
caseificación, es decir, un proceso de necrosis caseosa
que no difiere del de la osteítis tuberculosa;
-
cicatrización, es decir, un proceso de
transformación fibrosa retráctil que deja en el
hueso la huella de una típica cicatriz en forma
estrellada.
Las lesiones óseas sifilíticas producen, en
primer lugar, dolores locales profundos y lancinantes, que se
exacerban de noche y reciben el nombre de osteócopos,
porque dan la sensación al paciente de una rotura
ósea; el hueso – generalmente la tibia, el
esternón, la clavícula, etcétera – empieza a
engrosarse lentamente formando una tumefacción
circunscrita o difusa indolora, no caliente y cubierta de piel
normal.
Más tarde, al combinarse las lesiones anatómicas
de carácter destructivo y neoformador,
aparecen las típicas deformaciones a cargo de la calota
craneal, de la nariz, etc., como las que hemos descrito a
propósito de la sífilis congénita.
El diagnóstico de las lesiones óseas
sifilíticas se basa en las características
morfológicas descritas, en los típicos dolores
osteócopos, en los antecedentes sifilíticos del
individuo, en
la eventual coexistencia de lesiones sifilíticas
viscerales, en la positividad de las reacciones
serológicas, en las características
radiológicas de la osteítis luética,
etcétera. En todo caso, cuando aún subsiste la duda
se practicará un tratamiento antisifilítico
(penicilina, arsenobenzoles), el cual, al mejorar las lesiones
óseas, nos asegurará el carácter
sifilítico de las mismas.
Osteítis leprosa (o lepra del hueso)
En el curso de la lepra tuberosa o nodular, la
infección se puede localizar en los pequeños huesos
de la mano y del pie: los bacilos de la lepra alcanzan el hueso
por la vía hematógena (sanguínea) o por los
LEPROMAS de las partes blandas en contacto inmediato con el
hueso.
Los bacilos de Hansen, al implantarse primitivamente en la
médula interna del hueso o en la membrana del periostio
que los envuelve, provocan la destrucción lenta y limitada
del tejido óseo por la acción osteoclástica
producida por el tejido de granulación específico
leproso (leproma) que se forma en el hueso infectado.
También en la lepra nerviosa o anestésica pueden
presentarse alteraciones óseas de los pequeños
huesos de la mano y de los pies, e incluso del esqueleto nasal;
pero no están provocados por la implantación de los
bacilos leprosos sobre el hueso, sino que son la consecuencia de
los fenómenos de atrofia progresiva del hueso, por las
alteraciones nutritivas consecutivas a las lesiones de los
nervios locales. En los casos más graves, la atrofia puede
producir hasta la total desaparición del hueso (lepra
mutilante).
El tratamiento contra la osteítis leprosa es
sustancialmente idéntico al de la infección leprosa
en general (ver Lepra).
Osteítis micóticas o fungosas u Osteomicosis (o
Micosis óseas). -En los huesos pueden desarrollarse muchos
hongos
patógenos, provocando une serie de formas de
osteítis micóticas o fungosas: actinomicosis,
esporotricosis, aspergilosis, blastomicosis, etc. De todas estas
micosis óseas, la forma más frecuente e importante
es la actinomicosis. De las demás sólo indicaremos
que la esporotricosis ósea afecta preferentemente a los
huesos largos de las extremidades, localizándose
primitivamente en la médula interna o en el periostio
periférico, y provocando la formación dé
típicos nodulos de granulación específica
(esporotricomas) que destruyen lentamente el hueso por
demolición osteoclástica, sobreviniendo la fusión
purulenta con formación de pus que tiende a evacuarse
hacia el exterior mediante una fístula; en el pus se
encuentran numerosos hongos.
La aspergilosis, la blastomicosis y la hemisporosis del hueso
provocan también la formación de tejido
específico de granulación, que después de
haber erosionado más o menos lentamente el tejido
circundante sufre una fusión purulenta, evacuándose
el pus formado hacia el exterior a través de una
fístula.
La actinomicosis ósea (u osteítis
actinomicótica) es solamente una de las varias
localizaciones de este hongo parásito en el organismo (el
actinomyces bovis); existen también formas de
actinomicosis cutánea, nasal, pulmonar, intestinal,
pleural, pericárdica, peritoneal y hasta cerebral. En
todas estas diversas localizaciones – para las cuales nos
remitimos a la palabra Actinomicosis – la lesión
fundamental histológica es el característico
actinomicoma, es decir, una pequeña masa de tejido de
granulación específica – formado por capilares
sanguíneos, células
linfoides, epiteliales, histiocitarias y grandes células
cargadas de lipoides – que se forma en el seno del tejido
invadido para destruirlo más o menos lentamente y provocar
una fusión purulenta.
En relación con la actinomicosis ósea diremos
que el hueso más frecuentemente afectado es la
mandíbula inferior y también la superior; la
vía de penetración del hongo parásito – el
actinomyces bovis, que se encuentra en la hierba fresca o en el
heno, a partir del cual infecta a los bóvidos (en los
cuales este proceso abunda mucho más que en el hombre) y
también a los agricultores – suele ser la mucosa gingival
o un diente careado. Una vez penetrado en la sangre, el
actinomyces puede implantarse, arrastrado por la corriente
sanguínea, en una vértebra, en una costilla,
etc.
En el seno del hueso afectado aparecen muchos
tubérculos duros (que corresponden a otros tantos
actinomicomas), los cuales erosionan lentamente el tejido
óseo circundante y después sufren la fusión
purulenta con formación de pus que tiende a salir al
exterior a través da uní fístula excavada en
los tejidos blandos; en el pus se suele descubrir, a la observación microscópica, el
característico actinomyces.
Cuando la osteítis actinomicótica no regresa
mediante el tratamiento con yoduro potásico a dosis
elevadas, se debe recurrir a la intervención
quirúrgica del hueso lesionado: extirpación del
foco actinomicótico con amplias incisiones y raspado,
colocando gasa yodofórmica a lo largo del trayecto
fistuloso.
Osteítis parasitarias
Son las provocadas por la implantación del Quiste del
equinococo sobre un hueso. La tenia del equinococo – para cuya
descripción nos remitimos a la palabra Equinococo – es un
verme aplanado de algunos centímetros de longitud, que
vive en estado adulto en el intestino del perro o del gato, pero
que puede infectar, como huésped intermedio, al hombre cuando
ingiere accidentalmente los huevos del gusano; al llegar al
intestino humano estos huevos se abren y dejan en libertad una
serie de embriones que perforan las paredes intestinales y
penetran en la circulación sanguínea, a
través de la cual van a enquistarse en el hígado,
los pulmones, el bazo, el páncreas, los riñones el
cerebro, etc., e
incluso los huesos, provocando los respectivos quistes.
El quiste óseo del equinococo, según las
diversas estadísticas, representa aproximadamente el
2-3% de todos los casos de quiste del equinococo orgánico.
Los huesos que más se afectan son los de la pelvis
(ilíaco, sacro), de la columna vertebral y de las
extremidades inferiores (fémur, tibia, etc.). El
parásito se implanta primitivamente en el interior del
hueso, entre las trabéculas de su parte esponjosa, e
inicia un proceso de lenta e implacable destrucción
progresiva del hueso circundante mediante su desarrollo expansivo
excéntrico: tanto es así, que el hueso puede quedar
reducido a una delgada capa periférica de tejido compacto
con el resto completamente destruido.
En algunas ocasiones puede presentarse la perforación
de esta sutil " corteza" con la consiguiente inundación y
colonización quística del periostio y de los
músculos vecinos. Es natural que un hueso
tan erosionado y minado en su interior se deforme bajo el peso
del cuerpo y se fracture con gran facilidad por la acción
de los traumas de una cierta intensidad.
El tratamiento de esta grave osteítis por quiste
hidatídico es únicamente quirúrgico:
abertura de la cavidad patológica formada en el interior
del hueso y raspado de sus paredes al objeto de extirpar el
tejido óseo circundante lesionado por el proceso erosivo.
Pero con cierta frecuencia es preciso extirpar todo el hueso o
una porción más o menos extensa del mismo.
Osteítis tóxicas o por venenos– Varias
intoxicaciones
crónicas externas – por mercurio,
ácido crómico, arsénico, polvos de
nácar, etc., y sobre todo por el fósforo – pueden
producir, en forma lentamente progresiva, la muerte
(necrosis) del tejido óseo.
La osteoperiostitis mercurial.- no infrecuente en los
mineros y operarios que extraen o maní pulan el mercurio y
en los individuos que practican tratamientos mercuriales muy
prolongados y a dosis elevadas – se localiza únicamente en
los dos maxilares y es consecutiva a estomatitis y gingivitis
graves; en efecto, después de haber necrotizado gravemente
el revestimiento gingival, el veneno ataca a los dientes (caries)
y después al tejido óseo de las dos
mandíbulas en las que están excavados los
alvéolos de los dientes.
El hueso se necrosa lentamente por la acción
tóxica directa del mercurio sobre el tejido óseo y
sobre la membrana del periostio que lo envuelve y lo nutre.
El tratamiento consiste en alejar al operario de su trabajo o en
la suspensión inmediata de la cura mercurial en el
individuo sifilítico.
La osteoperiostitis fosfórica era, hasta hace unos
años, bastante frecuente entre los operarios de las
fábricas de cerillas por la absorción de los
vapores del fósforo blanco manipulado; en estos
últimos años, la instauración de la
profilaxis adecuada contra esta forma grave de
intoxicación crónica profesional ha hecho que sea
mucho más rara la osteoperiostitis fosfórica. Se
manifiesta lentamente apareciendo únicamente en los
operarios que llevan cinco años expuestos a la
inhalación de los vapores de fósforo blanco. Las
lesiones gingivales (piorrea) y dentarias (caries penetrante)
favorecen la aparición de la osteoperiostitis, que prende
sobre todo en el tejido óseo de las dos mandíbulas.
Se trata de un proceso inexorablemente progresivo que puede
destruir casi todo el hueso; en los casos más graves el
proceso destructivo puede extenderse hasta los huesos de la base
del cráneo (esfenoides, etmoides) determinando la
aparición de trastornos meningoencefálicos por
irritación e inflamación de las meninges cerebrales
y de la parte inferior de la masa cerebral.
La osteoperiostitis tiene inicialmente los caracteres de una
lesión inflamatoria y más tarde adquiere una
evolución necrótica, es decir, de
desvitalización y destrucción del tejido
óseo inflamado; además de este proceso
necrótico destructivo se puede producir también una
osteogénesis, es decir, la formación de un nuevo
tejido óseo que repare parcialmente el destruido.
El carrillo del paciente se presenta notablemente hinchado por
la reacción inflamatoria y con uno o más trayectos
fistulosos, a través de los cuales fluye un líquido
purulento y fétido que representa el término del
proceso destructivo del hueso; pequeños trozos de
éste, de color negruzco,
se encuentran con cierta frecuencia en el pus. Las encías
están frecuentemente enrojecidas y sanguinolentas y los
dientes acaban cayéndose.
La enfermedad provoca fuertes dolores locales, sobre todo en
el período inicial cuando el diagnóstico de la
enfermedad no se ha hecho en la gran mayoría de los
casos.- Se piensa entonces en dolores de origen dentario, con
irradiaciones de tipo neurálgico a lo largo de la
mandíbula; cuando a pesar de la extirpación de uno
o más dientes el dolor no se calma, es cuando se piensa
«mi el proceso osteítico de ambos maxilares.
El tratamiento de esta grave osteoperiostitis necrótica
por el fósforo consiste en el alejamiento del operario de
su labor cuando aparezcan los primeros síntomas. Cuando la
enfermedad está desarrollada, el tratamiento comprende los
siguientes apartados:
1) Desinfección total de la cavidad bucal, en la
que vive una flora polimicrobiana que puede provocar infecciones
secundarias sobre los tejidos blandos inflamados de los carrillos
y en el tejido óseo maxilar en vías de esfacelo
necrótico.
2) Tratamiento quirúrgico sobre el hueso
lesionado, mediante el drenaje escrupuloso de las fístulas
abiertas y extirpación de los llamados " secuestros"
óseos, es decir, de las porciones de tejido óseo
desvitalizadas y muertas.
En los casos más graves se procederá a la
resección precoz de la zona lesionada del hueso maxilar al
objeto de salvar la parte sana del mismo. Sólo en una
segunda fase, cuando el proceso osteítico esté
dominado, se practicarán las intervenciones
quirúrgicas para reparar las graves deformaciones locales
de orden estético y funcional (masticación).
ENFERMEDAD DE
PAGET
DESCRIPCIÓN
La enfermedad de Paget (osteítis deformans) fue
descrita por primera vez en 1876 en una reunión de la
Sociedad
Médico Quirúrgica en Inglaterra por
Sir James Paget, un cirujano británico bien conocido.
Conocida como enfermedad de Paget, esta enfermedad ósea no
debe ser confundida con la enfermedad de Paget de la mama o de la
vulva que son dos condiciones malignas que también llevan
el nombre de este médico.
Esta enfermedad se caracteriza por una excesiva
resorción ósea por los osteoclastos seguida de una
sustitución de la médula por un tejido vascular
conectivo fibroso, mientras que el hueso perdido es sustituido
por hueso trabecular dispuesto de una manera desorganizada. La
deposición del hueso neoformado, que ocurre frecuentemente
en forma de láminas, es la responsable del aspecto de
mosaico o rompecabezas del hueso. Este desorden está
usualmente localizado pero en ocasiones puede ser
generalizado.
EPIDEMIOLOGÍA
La prevalencia de la enfermedad de Paget es sustancial en
algunas áreas (es muy frecuente en Inglaterra, Estados
Unidos, Australia y Europa
occidental) mientras que en otras es extremadamente rara
(India,
China,
Japón y
Escandinavia). En Inglaterra, la prevalencia de la enfermedad
demostrada radiográficamente es <1%. En las autopsias,
la prevalencia es del 3 al 5% y aumenta a medida que aumenta la
edad de la muestra.
Usualmente el diagnóstico se lleva a cabo a partir de los
50 años y es casi igual en hombres y mujeres con un ligero
predominio de las últimas.
La historia
familiar puede ser positiva para la enfermedad de Paget en casi
un 40% de los sujetos y en algunas de estas familias, la
enfermedad está ligada a un locus del cromosoma 18.
ETIOLOGÍA
No se conocen las causas de la enfermedad. Algunas de sus
manifestaciones pueden ser suprimidas con glucocorticoides,
salicilatos y fármacos citotóxicos pero no hay
evidencia de que se trate de un proceso inflamatorio. El hecho de
que se hayan encontrado inclusiones en el citoplasma y
núcleo de los osteoclastos que se asemejan a las
nucleocápsides del virus de la
rubéola, con positividad de los anticuerpos monodonales
hacia los antígenos de los paramixovirus, sugieren un
origen infeccioso por estos virus.
Evidencia adicional de que los virus de la rubéola
podrían estar implicados en la génesis de la
enfermedad son los resultados de algunos estudios in vitro en los
que células CD34+ derivadas de
médula ósea normal transducidas con el gen de la
nucleocápside del virus de la rubéola se
diferencian en osteoclastos polinucleados que reabsorben hueso.
Sin embargo, la distribución universal de los paramixovirus
y la localización preferente en determinadas áreas
geográficas hace pensar que debe intervenir,
adicionalmente, algún factor genético.
Se ha detectado enfermedad de Paget en familias, estando
afectados individuos de varias generaciones con un patrón
hereditario consistente con una transmisión autosomal
dominante. En algunas familias se ha mapeado la enfermedad en el
locus 18q21-22, pero no en otras, lo que indica una heterogenidad
genética.
ANATOMÍA PATOLÓGICA
La principal característica de la enfermedad es un
aumento de la resorción y de la formación de hueso.
En su fase precoz, la resorción predomina con lo se pierde
densidad
ósea. Esta fase de denomina a menudo fase destructiva u
osteoporótica y suele cursar con un balance de calcio
negativo. Este predominio de la resorción va seguida de la
formación de hueso nuevo, progresivamente más denso
a medida que se reduce la resorción llegándose
finalmente a un balance de calcio positivo. La
remodelación ósea está enormemente aumentada
en la fase precoz de la enfermedad, hasta 20 veces su valor
normal.
El hueso pagétíco se caracteriza
macroscópicamente por la presencia de lesiones
líticas acompañadas de deformaciones
hipertróficas generalizadas. Microscópicamente se
observa un aumento en el número y tamaño de los
osteoclastos, con múltiples núcleos
pleomórficos. Cuando se estudia el hueso de las lesiones
blásticas se observa un tejido desestructurado con
líneas de cemento
entrecortadas que parecen un mosaico. Se observa un incremento en
la producción de interleukina L6 y las células son
más sensibles de lo normal a los efectos pro-resortivos de
la 1,25 (OH)2-D3.
La mayor remodelación ósea se correlaciona con
un aumento de los niveles de fosfatasa alcalina que son
más altos en la enfermedad de Paget que en cualquier otro
caso (excepto en el caso de una hiperfosfatasemia hereditaria).
Las concentraciones de calcio y fosfato son normales debido la
deposición de estas sustancias sobre el hueso neoformado y
por la regulación de la hormona paratiroidea.
La resorción ósea implica no solo sustancias
minerales sino
también orgánicas y productos como
la hidroxiprolina o complejos de hidroxipiridio que no son
reutilizados para la formación de hueso nuevo y que se
eliminan en la orina. Los compuestos de piridinio piridinolina
(Pyr) y deoxipirídinolina (D-Pyr) liberados del
colágeno durante la resorción osteoclástica
se utilizan como marcadores para diagnosticar la condición
aunque suele ser suficiente la determinación de la
fosfatasa alcalina que está muy aumentada.
HALLAZGOS RADIOLÓGICOS
Los hallazgos radiológicos se centran sobre todo en el
fémur, cráneo, tibia, espina lumbrosacra,
clavículas y costillas. Los huesos pequeños no son,
por el general afectados. Los más característicos
se encuentran en el raquis y el cráneo: en el raquis se
puede observar una trabeculación basta vertical o
áreas de esclerosis en banda en las plataformas. En el
cráneo se observan zonas radiolucentes en los huesos
frontales, parietales y occipitales.
En la fase avanzada hay un ensanchamiento y engrosamiento de
todo el cráneo con zonas con manchas de mayor densidad. En
los huesos largos, se observan frecuentemente zonas
perpendiculares radiolucentes sobre todo en la parte convexa de
la tibia y el fémur, que representan zonas
líticas. Los cambios en la pelvis reflejan la
variación de la resorción ósea y
formación de hueso nuevo y a menudo va acompañada
de un engrosamiento en las alas de la misma.
PRUEBAS DE LABORATORIO
La remodelación ósea altera las pruebas de
laboratorio
relacionadas con la formación ósea como son la
fosfatasa alcalina y la osteocalcina y tas de la resorción
como son la hidroxiprolina. Las medidas de la proteína C
reactiva y del telopéptido N son también
útiles para determinar la evolución de la
enfermedad cuando esta está en fase avanzada.
MANIFESTACIONES CLÍNICAS
Las manifestaciones clínicas de la enfermedad de Pager,
depende del estadio de la enfermedad y de los huesos que
están implicados. En la mayor parte de los casos la
enfermedad es asintomática y es descubierta cuando se
realizan radiografías de cabeza o de pelvis por otros
motivos o por comprobarse una elevación anormal de la
fosfatasa alcalina.
En otros sujetos se observa una hinchazón o
deformación de los huesos largos y desarrollan una cojera
debida a la diferencia en la longitud de las piernas. El
ensanchamiento del cráneo no es observado en la mayor
parte de los enfermos, a menos que usen sombrero. Muchos
individuos permanecen asintomáticos durante largos
períodos de tiempo, mientras que los sintomáticos y
con mayores niveles de hidroxiprolina en orina y de fosfatasa
alcalina sérica son los más propensos a la
aparición de nuevos síntomas. Estos son dolores
difusos de espalda y en las piernas que a veces pueden ser
agudos.
La localización cráneofacial conlleva
frecuentemente sordera por implicación directa de los
hueseciilos del oído
interno o por impacto sobre el octavo par craneal en el foramen
auditivo, cefaleas, epífora y excepcionalmente I dolores
neurálgicos. Puede producirse complicaciones más
serias de la enfermedad cuando el crecimiento óseo en la
base del cráneo (platibasia) comprime el cerebelo.
El flujo sanguíneo puede estar muy aumentado en las
extremidades afectadas por la enfermedad de Paget debido a la
elevada vascularización del hueso pagético, que va
acompañada por una vasodilatación cutánea
que se refleja en un aumento de temperatura
que se observa clínicamente. Cuando la enfermedad ha
progresado hasta implicar un tercio o más del esqueleto el
aumento del flujo de sangre ocasiona un aumento del gasto
cardíaco que raramente progresa a una insuficiencia
cardíaca.
Las fracturas patológicas pueden producirse en
cualquier estadio de la enfermedad aunque son más
frecuentes en la fase destructiva de la misma. Pueden producirse
espontáneamente o como consecuencia de cualquier trauma
ligero. Las fracturas completas son a menudo transversas como
sí el hueso se hubiera quebrado como un pedazo de
tiza.
Aunque la excreción de calcio no cambia
significativamente suele estar algo aumentada en la fase
resortiva lo que explicaría la mayor incidencia de
cálculos renales observada en estos pacientes. La
hiperuricemia y la gota son frecuentes en estos pacientes.
La complicación más grave es la
degeneración sarcomatosa cuya incidencia es ≤ 1% y es
la principal causa del sarcoma óseo del adulto. Los
sarcomas más frecuentes se observan en el fémur, el
húmero, el cráneo, los huesos faciales y en la
pelvis. La degeneración ósea se produce
generalmente en forma de osteosarcoma aunque también es
posible un fibrosarcoma o un condrosarcoma. La aparición
súbita de dolor muy intenso, aumento del dolor existente o
aumento explosivo de la fosfatasa alcalina puede hacer sospechar
de un sarcoma.
La confirmación radiológica puede ser
difícil por lo que se recurre a la TC y a la RMN. Los
tumores son multicéntricos en un 20% de los casos. Una vez
aparecido el tumor, la prognosis es mala: la cirugía
ablativa no suele tener muchos éxitos y los osteosarcomas
derivados de la enfermedad de Paget, rara vez responden a la
quimioterapia.
PUNTO ANALÍTICO
La EP no suele modificar el hemograma ni la VSG. La actividad
celular de la enfermedad altera las pruebas del laboratorio
relacionadas con la formación ósea, como la
fracción ósea de la fosfatasa alcalina y la
proteína Gla (osteocalcina), y las de resorción,
hidroxiprolinuria o la FART. Las elevaciones de estos
parámetros de resorción y/o formación
ósea traducen la situación de la enfermedad y
oscilan con ella. Así, son normales en las formas
inactivas y alcanzan cifras 20 ó 30 veces superiores en
fases muy activas de formas muy extensas. Tanto los datos
bioquímicos de formación (fosfatasa alcalina,
osteocalcina, procolágeno) como de resorción
ósea (hidroxiprolina, fosfatasa ácida, piridolina y
deoxipiridolina) suelen incrementarse, siendo parámetros
diagnósticos orientativos de la enfermedad.
De manera característica estos marcadores del recambio
óseo alterado se acompañan de una calcemia y una
fosforemia normales, al igual que la PTH inmunorreactiva. Algunos
pacientes con la enfermedad muy activa, inicialmente, pueden
presentar aumento de la calciuria y, rara vez, hipercalcemia
moderada. Sólo se observan estas hipercalcemias en fases
muy activas, en las degeneraciones sarcomatosas y en formas
moderadamente activas en pacientes inmovilizados. La enfermedad
se controla de manera objetiva mediante la observación de
los parámetros mencionados. Debe recordarse que los
parámetros biológicos de actividad son normales en
el nueve por ciento de los pacientes, correspondientes a formas
inactivas, y que casi la mitad de los casos cursa con elevaciones
de los parámetros de actividad superiores al 100 por
ciento de la normalidad.
Los reactantes de fase aguda, como la VSG y la proteína
C reactiva, sólo se alteran en formas muy extensas y muy
activas.
Aunque las mediciones de los valores
urinarios de los productos de la degradación del
colágeno proporcionan estimaciones válidas de
resorción del hueso, su aplicación clínica
es complicada debido a la pronunciada variabilidad
analítica y biológica. Por consiguiente, se han
desarrollado inmunoensayos para la determinación de tales
parámetros en suero.
En este estudio, los autores del artículo
evalúan la actuación de tres nuevos marcadores
séricos de actividad ósea, como los
telopéptidos séricos C-terminal y N-terminal del
colágeno tipo I (S-CTX y S-NTX) y la sialoproteína
ósea. Se compararon los resultados con las mediciones de
piridinolina urinaria total, la deoxipiridinolina total, con el
telopéptido C-terminal urinario de el colágeno tipo
I (U-CTX) y el telopéptidos N-terminal urinario del
colágeno tipo I (U-NTX). La población estudiada comprendía
hombres sanos (27), mujeres premenopáusicas (30) y
postmenopáusicas (31), pacientes con trastorno
hepático (24), fracaso renal (30), sin cáncer de
mama (24) y con cáncer mamario (30), metástasis
óseas, osteoporosis
vertebral primaria (27), hiperparatiroidismo primario (16),
enfermedad ósea de Paget activa (18), mieloma
múltiple (18), y pacientes con hipercalcemia de origen
maligno antes y después del tratamiento con pamidronato
(28). Los cambios en los marcadores séricos y urinarios
fueron similares en la mayoría de las enfermedades
óseas de origen metabólico.
Sin embargo, la diferencia de los niveles de los marcadores
séricos entre los controles sanos y los pacientes afectos
de osteoporosis vertebral primaria, o hiperparatiroidismo
primario, aumentó. En el mieloma múltiple, todos
los marcadores séricos y urinarios se elevaron
(p<0.05). En carcinoma de mama la afectación
ósea reflejó incrementos significativos en todo los
marcadores (p<0.01), exceptuando los valores de
U-CTX y S-CTX. En la hipercalcemia de origen maligno, los cambios
inducidos por el pamidronato en los biomarcadores eran
pronunciados para U-CTX y S-CTX y S-NTX. La disfunción
hepática y el fracaso renal se asociaban a niveles
elevados de todos los marcadores séricos (p<0.05). Los
autores afirman que las medidas séricas reflejan
resorción del hueso de una forma similar que las obtenidas
por mediciones de los marcadores urinarios. Puesto que los
marcadores de suero superan algunas de las limitaciones de los
marcadores urinarios, su uso mejora la valoración de las
patologías óseas.
TRATAMIENTO
Muchos pacientes no requieren tratamiento por estar la
enfermedad localizada y ser asintomática. El tratamiento
comienza a ser innecesario cuando hay complicaciones como dolor
persistente a algunos huesos, compresión neural,
deformidades óseas que afectan la marcha, hipercalciuria
severa con o sin formación de cálculos renales y la
repetición de fracturas.
Los fármacos antiinflamatorios no esteroídicos,
el paracetamol o los inhibidores de la COX2 pueden ser
útiles para aliviar el dolor. Los pacientes con dolores
severos de cadera o de rodilla pueden ser candidatos a una
sustitución de estas articulaciones.
Estas intervenciones conducen en muchos casos a excelentes
resultados.
Los bisfosfonatos pueden inhibir la resorción
ósea y son generalmente bien tolerados. El etidronato es
moderadamente efectivo aliviando los síntomas pero no
reduce los parámetros bioquímicos marcadores de la
enfermedad. El etidronato también inhibe la
mineralización ósea pero produce osteomalacia. Los
últimos bisfosfonatos como el tiludronato, el pamidronato,
el risedronato y sobre todo el alendronato son mucho más
potentes que el etidronato y no originan defectos en la
mineralización.
El alendronato y el risedronato se administran por vía
oral, pero son muy pobremente absorbidos por el tracto digestivo
y deben ingerirse en ayunas, 30 minutos antes de cualquier comida
para evitar una interferencia con los alimentos. El
pamidronato se utiliza por vía intravenosa en forma de
infusión a razón de 30 mg/día. Las
respuestas a estos bisfosfonatos son bastante rápidas y
los niveles urinarios de hidroxiprolina y compuestos de piridinio
caen rápidamente. La fosfatasa alcalina también
disminuye seguidamente. Estos cambios suelen ir
acompañados de fiebre que remite rápidamente.
Los pacientes tratados con
bisfosfonatos deben recibir suplementos de calcio (entre 1 y 1.5
g) y 400 U.I de vitamina D. En 6 meses de tratamiento, se
observan mejoras radiográficas sobre las lesiones
líticas.
La calcitonina se utiliza mucho menos desde la
introducción de los bisfosfonatos. Sin embargo, la
calcitonina es todavía útil en aquellos enfermos
que no toleran los bisfosfonatos. La administración de calcitonina humana, de
cerdo o de salmón reduce la hiperfosfatasemia alcalina y
la excreción urinario de hidroxiprolina. La administración de calcitonina disminuye el
dolor debido a la supresión de la lesión
pagética, pero también por mecanismo
analgésico central. Las dosis de calcitonina suelen ser de
50 a 100 UI diarias administradas por vía
subcutánea, aunque a veces es posible reducir las dosis a
3 días a la semana. Las dosis de la calcitonina en spray
nasal suelen ser de 200 UI/d.
OSTEOARTROPATÍA
PULMONAR HIPERTRÓFICA
DEFENICIÓN
La osteoartropatía pulmonar hipertrófica de
Bamberger-Pierre-Marie es una artritis seronegativa con
hipertrofia de falanges distales y acropaquias. Constituye un
síndrome osteoarticular, que no debe confundirse con los
dedos hipocráticos o dedos en palillo de tambor. Es menos
frecuente que las acropaquias.
Consiste en la asociación de acropaquias o dedos
hipocráticos con crecimiento subperióstico o
periostitis de los huesos largos, metacarpo, metatarso y
falanges. Cursa con dolor (a diferencia que las acropaquias),
hipersensibilidad, tumefacción y edema de los huesos
afectados. Los dolores son similares a los de la artritis
reumatoide y la piel es áspera y rugosa, con engrosamiento
de partes blandas.
EPIDEMIOLOGÍA
Aparece del 1 al 10% de los pacientes con cáncer de
pulmón, habitualmente adenocarcinoma de pulmón
(sobre todo) y carcinoma epidermoide de pulmón.
La causa más frecuente son los síndromes
paraneoplásicos sobre todo de cáncer de
pulmón, y en segundo lugar los procesos crónicos
del pulmón y también en mesoteliomas pleurales.
Disminuye al tratar el cáncer
y con AINE (antinflamatorios no esteroideos).
PATOGENIA
Es desconocida:
Un hecho significativo es que la sección de las fibras
vagales que inervan el pulmón se sigue de la
regresión de la osteoartropatía (en alguna
ocasión, esta misma respuesta se ha observado
después de seccionar las ramas somáticas
intercostales correspondientes a la localización del
tumor); por ello, se ha postulado que el tumor sea origen de
estímulos neurales, que, transportados por fibras
aferentes vagales, den lugar en el hipotálamo a una
respuesta, humoral o neural, hemodinámica, con aumento del
flujo sanguíneo a las partes distales de los miembros (en
la osteoartropatía hay una circulación
hiperdinámica) que sería responsable del
engrosamiento perióstico.
Otra teoría,
aunque puramente especulativa, mantiene que el tumor origina una
sustancia inductora de la hiperactividad perióstica, y que
se inactivaría en el pulmón (otra posibilidad
sería que en condiciones normales algunos tejidos, como el
bazo, la médula ósea o el riñón,
sinteticen una hormona estimuladora del periostio, que se
inactivara en el pulmón); esta teoría tiene una
base anatómica vascular que dice que en los tumores
pulmonares hay apertura de las anastomosis broncopulmonares, a
través de las cuales escaparían las
hipotéticas sustancias estimuladoras del periostio a su
inactivación pulmonar.
La realidad es que la patogenia de este síndrome sigue
sin estar aclarada, aunque su presentación asociada a un
tipo histológico concreto, el
carcinoma epidermoide, sugiere la existencia de un factor
humoral; el papel de las fibras vagales puede ser el de
conductoras de impulsos aferentes, o bien quizá tengan un
efecto eferente sobre el propio tumor, estimulando la
liberación del mencionado factor humoral.
OSTEÍTIS
FIBROQUÍSTICA
DEFINICIÓN
Descrita en 1891 por F. vonRecklinghausen.
Es una complicación del hiperparatiroidismo (demasiada
hormona paratiroides) en la cual los huesos se tornan blandos y
se deforman.
La osteítis fibrosa está caracterizada por la
reabsorción aumentada de hueso calcificado por los
osteoclastos y el reemplazo de hueso con tejido fibroso,
así como por el posible desarrollo de quistes. Puede ser
causada por hiperparatiroidismo primario (exceso en la
producción de la hormona paratiroidea).
PRINCIPALES EVIDENCIAS
MéDICAS
§ Aumento
de osteoclastos multinucleados en lagunas de Howship.
§
Sustitución de osteocitos y componentes de médula
ósea por tejido fibroso.
§
Formación de lesiones quísticas con contenido
fibroso (Tumores pardos)
§
Resorción perióstica de la cortical.
§
Lesiones osteolíticas
§
Cráneo en sal y pimienta
§
Tumoración de la glándula paratiroides como
compensación de la enfermedad ósea.
CAUSAS, INCIDENCIA Y FACTORES DE RIESGO
En el cuello existen 4 glándulas paratiroides, las
cuales producen paratirina que ayuda a controlar los niveles de
calcio en el cuerpo, al igual que incrementa la
descomposición del hueso (metabolismo
óseo). Demasiada cantidad de paratirina
(hiperparatiroidismo) puede llevar al incremento del metabolismo
de los huesos, lo cual puede causar su reblandecimiento.
Esta afección casi nunca es ocasionada por
cáncer de la paratiroides.
Antes de 1950, casi la mitad de las personas a quienes se les
diagnosticaba hiperparatiroidismo tenían osteítis
fibroquística. En la actualidad, esta afección no
es común, debido a que el diagnóstico de los
pacientes con hiperparatiroidismo se realiza de manera más
temprana, antes de que ocurra el reblandecimiento de los
huesos.
Las personas que tienen hiperparatiroidismo grave tienen un
riesgo mayor
de presentar osteítis fibroquística.
SÍNTOMAS
La osteítis fibroquística puede ocasionar dolor
o sensibilidad en los huesos y se pueden presentar fracturas
(rupturas) en los brazos, en las piernas o en la columna, al
igual que otros problemas
óseos.
El hiperparatiroidismo en sí mismo puede causar
cálculos o problemas renales, náuseas,
estreñimiento, fatiga y debilidad.
SIGNOS Y EXÁ MENES
Los exámenes de sangre muestran un alto nivel de
calcio, paratirina y fosfatasa alcalina (un químico de los
huesos). Los niveles de fósforo pueden estar bajos.
Las radiografías pueden revelar huesos delgados,
fracturas, arqueamiento y quistes. Asimismo, las
radiografías dentales pueden ser anormales.
Se puede tomar una radiografía del hueso, dado que las
personas con hiperparatiroidismo tienen más probabilidad
de padecer osteopenia (huesos delgados) u osteoporosis (huesos
muy delgados) que de padecer osteítis fibrosis
completamente desarrollada.
Tratamiento
El principal tratamiento para el hiperparatiroidismo es la
cirugía de extirpación de la(s) glándula(s)
paratiroides anormal(es). Algunas de las técnicas
más modernas incluyen el uso de trazadores radiactivos y
la realización de exámenes de sangre para hormona
paratiroidea rápidos para que la cirugía sea
más fácil y más ágil. Si no es
posible realizar una cirugía, algunas veces se pueden
utilizar medicamentos para disminuir los niveles de calcio.
COMPLICACIONES
Algunas de las complicaciones de la osteítis fibrosa
son las fracturas, dolor y deformidades de los huesos.
También se pueden presentar otros problemas a causa del
hiperparatiroidismo en sí, tales como cálculos
renales e insuficiencia del riñón, situaciones que
requieren asistencia médica.
Se debe buscar asistencia médica si se detecta dolor o
sensibilidad en los huesos o si se tienen una fractura o
cualquier otro síntoma de hiperparatiroidismo.
CONCLUSIONES
La osteítis es una inflamación causada por
diversos entes tales como las bacterias,
hongos, parásitos y algún tipo de sustancia
tóxica o veneno.
La osteítis se presenta en enfermedades
sistémicas esqueléticas, siendo éstas de
importancia médica e investigación.
Algunas Imágenes
de la enfermedad de Paget
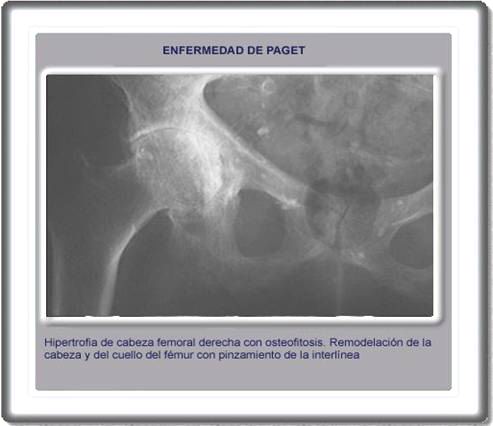




PAGET
REFERENCIAS
BIBLIOGRÁ FICAS
- Lewallen DG. Hip arthroplasty in patients with Paget's
disease.Clin Orthop 1999. - Singer FR. Update on the viral etiology of Paget's disease
of bone.1999 Octubre. - Selby PL. Pamidronate in the treatment of Paget's
disease.1999 Mayo. - Eastell R. Biochemical markers of bone turnover in Paget's
disease of bone.1999 Mayo. - Altman RD. Paget's disease of bone: rheumatologic
complications. 1999 Mayo. - Kaplan FS. Severe orthopaedic complications of Paget's
disease. 1999 Mayo. - Roodman GD. Mechanisms of abnormal bone turnover in Paget's
disease 1999 Mayo. - Cooper C, Dennison E, Schafheutle K, Kellingray S, Guyer P,
Barker D. Epidemiology of Paget's disease of bone.1999
Mayo. - Van Hul W. Paget's disease from a genetic perspective.1999
Mayo. - Mee AP. Paramyxoviruses and Paget's disease: the
affirmative view.1999 Mayo. - Ralston SH, Helfrich MH. Are paramyxoviruses involved in
Paget's disease? A negative view.1999 Mayo. - Nuevo Manual Merck de
información médica general.
Editorial Océano. 2003. España.
2ª edición. Vol. I
Autor:
Montero Carbajal Tatiana Lizzeth
Nieto Polo Salinas Maria Susana
Ñique García Lucía Carolina
 Página anterior Página anterior |   Volver al principio del trabajo Volver al principio del trabajo | Página siguiente  |
