- Fundamento
teórico - Parte
experimental - Tratamiento de
datos - Análisis de
resultados - Conclusiones
- Bibliografía
Objetivos
Aprender la importancia de la determinación
de la alcalinidad del agua para diferentes
procesos.Determinación de campo de la alcalinidad
total y parcial.
Fundamento
teórico
Es importante conocer la alcalinidad del agua para
realizar procesos de
ablandamiento por precipitación, para saber la cantidad de
cal y sosa que se debe dosificar.
La alcalinidad significa la capacidad tampón del
agua; la capacidad del agua de neutralizar.
Evitar que los niveles de pH del agua
lleguen a ser demasiado básico o ácido. La
alcalinidad estabiliza el agua en los
niveles del pH alrededor de 7. Sin embargo, cuando la acidez es
alta en el agua la alcalinidad disminuye, puede causar
condiciones dañinas para la vida
acuática.
En química del agua la
alcalinidad se expresa en PPM o el mg/l de carbonato equivalente
del calcio. La alcalinidad total del agua es la suma de las tres
clases de alcalinidad; alcalinidad del carbonato, del bicarbonato
y del hidróxido.
La alcalinidad se debe en mayor parte por el CO2 que
absorbe el agua en su trayecto o estancada, las reacciones que se
dan son las siguientes:
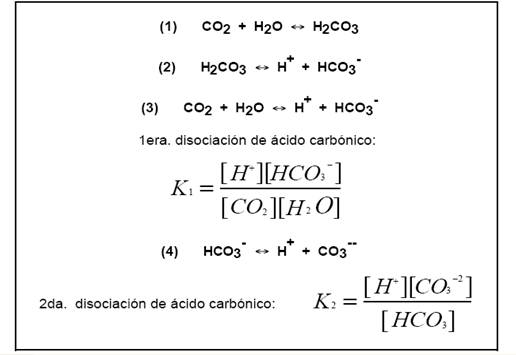
Existe una relación entre la alcalinidad, el pH y
los iones presentes:

También lo podemos ver de la siguiente forma: el
efecto del pH en la concentración de especies carbonatas
en el agua:

Existen dos tipos de alcalinidad, que representan el pH
y la cantidad de carbonatos o bicarbonatos presentes como se
muestras en la grafica anterior, así como también
el OH- presente.
Alcalinidad total (M o T): que representa el
total de iones que intervienen, se determina con el indicador
anaranjado de metilo:

Alcalinidad parcial (P): que representa solo
algunos de los iones que intervienen, se determina con el
indicador anaranjado de metilo:

Parte
experimental
Muestra 1: Agua de Pozo
Alcalinidad P: se tomo una muestra de 5 ml y
se agrego dos gotas del indicador P (fenolftaleina), no
presentó cambio de
color, por lo que
la alcalinidad P es cero.
Alcalinidad M: se tomo una muestra de 5 ml y se
agrego dos gotas del indicador M (el indicador utilizado no
era el anaranjado de metilo), presentó una
coloración azul, luego se agrego la solución
titulante 3.2 mmoles hasta que cambio de color a rojo.
Muestra 2: Agua del TK de Condensado
Alcalinidad P: se tomo una muestra de 5 ml y se
agrego dos gotas del indicador N°1 (fenolftaleina), no
presentó cambio de color, por lo que la alcalinidad P es
cero
Alcalinidad M: se tomo una muestra de 5 ml y se
agrego dos gotas del indicador M (el indicador utilizado no
era el anaranjado de metilo), presentó una
coloración azul, luego se agrego la solución
titulante 18.3 mmoles hasta que cambio de color a
rojo.
Muestra 3: Agua de Caldera
Alcalinidad P: se tomo una muestra de 5 ml y se
agrego dos gotas del indicador M (fenolftaleina), si hubo viraje
del indicador dando 13.7 mmoles de la solución
titulante.
Alcalinidad M: se tomo una muestra de 5 ml y se
agrego dos gotas del indicador M (el indicador utilizado no
era el anaranjado de metilo), presentó una
coloración azul, luego se agrego la solución
titulante 2.5 mmoles hasta que cambio de color a rojo.
Tratamiento de
datos

Por lo tanto para hallar la alcalinidad se utiliza la
siguiente formula:

Como las muestras no presentaron alcalinidad P,
calculamos la alcalinidad M para los tres puntos de
recolección:

Con el siguiente cuadro podemos hallar las
concentraciones de los distintos iones en las
muestras:

Entonces tenemos el siguiente resultado:

Análisis
de resultados
Página siguiente  |
